Alimlər nəhayət otaq temperaturunda qaz faza reaksiyası vasitəsilə sabit neytral azot allotropunu sintez etdilər
Azot, nəhayət, bir kimyəvi elementin müxtəlif struktur formaları olan neytral allotroplar yarada bilən karbon kimi elementlərin elit təbəqəsinə qoşulur. Justus Liebig Universitetinin tədqiqatçıları, Gissen, Almaniya, neytral heksanitrogen (N 6 ) sintez etdilər – 18-ci əsrdə təbii olaraq meydana gələn dinitrogenin (N 2 ) kəşfindən bəri ilk neytral azot allotropu, kriogen cəhətdən sabitdir və otaq temperaturunda hazırlana bilər.
Təbiətdə nəşr olunan bu yeni araşdırma, qaz faza reaksiyası vasitəsilə heksanitrogen (N 6 ) sintez etdi, əsas maddələr xlor (Cl 2 ) və ya brom (Br 2 ) və son dərəcə reaktiv və partlayıcı bərk gümüş azid (AgN 3 ) ilə aşağı təzyiq altında.
Tədqiqatçılar AgN 3-ü daxili səthə yaydılar və qaz halogeni (Cl 2 və ya Br 2 ) otaq temperaturunda azaldılmış təzyiq altında bərkdən keçdi. Prosesin törətdiyi reaksiya xloronitrenin (ClN) və hidrazoy turşusunun (HN 3 ) yan məhsulları ilə yanaşı N 6 əmələ gətirir .
Bu molekullar daha sonra yüksək reaktiv N 6-nı sabitləşdirmək və təcrid etmək üçün kriogen şəraitdə (10 Kelvin) bərk arqonun inert matrisi olan arqon matrislərində tutuldular .
Azotun molekulyar formaları karbon-neytral və yüksək enerji sıxlığı olan materiallar kimi yüksək perspektivlidir. Parçalandıqdan sonra onlar CO 2 kimi istixana qazları yaradan ənənəvi yanacaqlardan fərqli olaraq, sabit N 2 formasına, qeyri-toksik, inert qaza parçalandıqları üçün böyük miqdarda enerji buraxırlar .
Təəssüf ki, N 2 azotun yeganə təbii allotropudur (molekulyar formasıdır), qeyri-adi güclü üçlü bağlardan yaranan inert təbiətinə görə yanacaq kimi istifadə üçün yararsızdır.

Onilliklər ərzində elm adamları daha böyük neytral azot molekullarını enerji materialları kimi sintez etməyə çalışdılar, lakin polinitrogen molekullarının son dərəcə qeyri-sabit təbiəti səbəbindən uğursuz oldular.
Əvvəlki tədqiqatlar azid radikalını (-N 3 ) və ikinci N 4-ü spektroskopiya yolu ilə aşkar etmişdi, lakin onların strukturu sirr olaraq qaldı. Nəzəri cəbhədə N 4- dən N 12- ə qədər olan strukturlar proqnozlaşdırılıb, lakin heç biri eksperimental olaraq təcrid olunmayıb, çünki onlar çox qeyri-sabit hesab olunurlar.
https://googleads.g.doubleclick.net/pagead/ads?gdpr=0&us_privacy=1—&gpp_sid=-1&client=ca-pub-0536483524803400&output=html&h=280&slotname=8188791252&adk=1645945215&adf=2612643799&pi=t.ma~as.8188791252&w=750&abgtt=6&fwrn=4&fwrnh=0&lmt=1750222631&rafmt=1&armr=3&format=750×280&url=https%3A%2F%2Fphys.org%2Fnews%2F2025-06-scientists-stable-neutral-nitrogen-allotrope.html&fwr=0&rpe=1&resp_fmts=3&wgl=1&uach=WyJXaW5kb3dzIiwiMTkuMC4wIiwieDg2IiwiIiwiMTM3LjAuNzE1MS4xMDQiLG51bGwsMCxudWxsLCI2NCIsW1siR29vZ2xlIENocm9tZSIsIjEzNy4wLjcxNTEuMTA0Il0sWyJDaHJvbWl1bSIsIjEzNy4wLjcxNTEuMTA0Il0sWyJOb3QvQSlCcmFuZCIsIjI0LjAuMC4wIl1dLDBd&dt=1750222631512&bpp=4&bdt=188&idt=46&shv=r20250616&mjsv=m202506110101&ptt=9&saldr=aa&abxe=1&cookie=ID%3Df22668bce9793ae4%3AT%3D1735196613%3ART%3D1750222397%3AS%3DALNI_Mb4Xpwl1SO1AcvqroR6xccDm_sheQ&gpic=UID%3D00000f7c5320f40b%3AT%3D1735196613%3ART%3D1750222397%3AS%3DALNI_Mb1dz_DHiT2yDzXLMaB9CDkQl4XGg&eo_id_str=ID%3Dcdf7f2f01784f52d%3AT%3D1735196613%3ART%3D1750222397%3AS%3DAA-Afjb8kbeupLLyQ0QHQmZxpM4v&prev_fmts=0x0%2C336x280%2C1200x280&nras=1&correlator=6682577583236&frm=20&pv=1&rplot=4&u_tz=240&u_his=3&u_h=1080&u_w=1920&u_ah=1032&u_aw=1920&u_cd=24&u_sd=1&dmc=8&adx=448&ady=2196&biw=1905&bih=945&scr_x=0&scr_y=0&eid=31092113%2C31092960%2C95353386%2C95362656%2C95362800%2C95359266%2C95362809%2C95363074%2C31091638&oid=2&pvsid=374324948025821&tmod=2074743607&uas=0&nvt=1&ref=https%3A%2F%2Fphys.org%2F&fc=1920&brdim=0%2C0%2C0%2C0%2C1920%2C0%2C1920%2C1032%2C1920%2C945&vis=1&rsz=%7C%7CpeEbr%7C&abl=CS&pfx=0&fu=128&bc=31&bz=1&td=1&tdf=2&psd=W251bGwsbnVsbCxudWxsLDNd&nt=1&ifi=5&uci=a!5&btvi=3&fsb=1&dtd=115
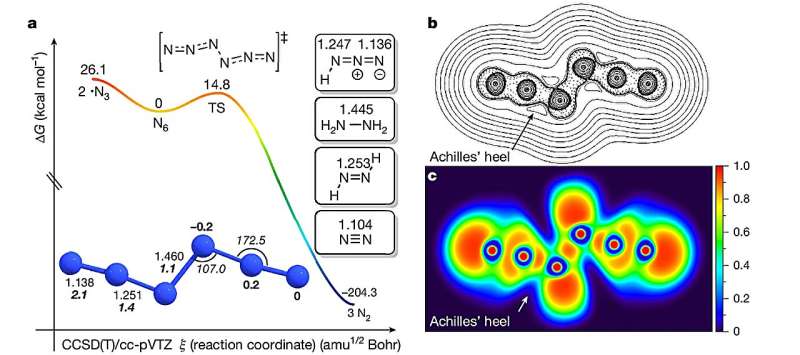
Bu tədqiqat təkcə neytral N 6 molekulunu uğurla sintez etməklə deyil, həm də onun xətti, asiklik quruluşunu C 2h simmetriyası ilə müəyyən etməklə tendensiyanı pozdu . Molekul, iki azid (N 3 ) vahidi və üç azot atomunun mərkəzdə tək N-N bağı ilə birləşdirilən qoşa bağlarla bir yerdə tutulduğu altı azot atomu zəncirindən ibarətdir .
Mexanizm, ehtimal ki, iki addımlı qaz fazalı reaksiyanı əhatə edirdi. Əvvəlcə qaz halında olan Cl 2 və ya Br 2 gümüş azidlə reaksiyaya girərək gümüş halid (AgX, burada X = Cl və ya Br) və halogen azid (XN 3 ) əmələ gətirir. Birinci mərhələdə əmələ gələn halogen azid gümüş azidin başqa bir molekulu ilə reaksiyaya girərək gümüş halid və heksanitrogen (N 6 ) əmələ gətirir.

Otaq temperaturunda istehsal edilən N 6 kriogen temperaturda sabit qaldı və tədqiqatçılara onu 77 K-də təmiz film kimi təcrid etməyə imkan verdi – azotun mayeyə çevrildiyi temperatur. Hesablama hesablamaları molekulun yarı ömrünün otaq temperaturunda 35,7 millisaniyə, kriogen şəraitdə isə 132 ildən çox olduğunu ortaya qoydu.
Tədqiqatçılar həmçinin aşkar etdilər ki, N 6 parçalandıqda müstəsna miqdarda enerji buraxır – məlum partlayıcı TNT-dən 2,2 dəfə və RDX-dən iki dəfə çox vahid kütləyə.
Onlar vurğulayırlar ki, N2- dən kənarda metastabil molekulyar azot allotropunun hazırlanması nəinki fundamental elmi anlayışı inkişaf etdirir, həm də gələcək enerji saxlama tətbiqləri üçün potensiala malikdir.
Müəllifimiz Sanjukta Mondal tərəfindən sizin üçün yazılmış , Sadie Harley tərəfindən redaktə edilmiş və Robert Eqan tərəfindən yoxlanılmış və nəzərdən keçirilmiş bu məqalə diqqətli insan əməyinin nəticəsidir. Müstəqil elmi jurnalistikanı yaşatmaq üçün sizin kimi oxuculara güvənirik. Bu hesabat sizin üçün əhəmiyyət kəsb edirsə, lütfən, ianə (xüsusilə aylıq) nəzərdən keçirin. Siz təşəkkür olaraq reklamsız hesab əldə edəcəksiniz .
Daha çox məlumat: Weiyu Qian et al, Neytral azot allotropunun heksanitrogen C 2h -N 6 hazırlanması , Təbiət (2025). DOI: 10.1038/s41586-025-09032-9
Jurnal məlumatı: Təbiət
© 2025 Science X Network