Alimlər yeni alət ‘scICE’ ilə tək hüceyrəli məlumatların etibarlılıq böhranını həll edirlər
Təkhüceyrəli RNT ardıcıllığı (scRNA-seq) kimi tanınan tək hüceyrə səviyyəsində gen ifadəsini təhlil etmək bacarığı immunologiya, onkologiya və inkişaf biologiyası üzrə kəşflərə təkan verən həyat elmlərini dəyişdirdi. 40.000-dən çox tədqiqat toxumalar və orqanizmlər daxilində hüceyrələrin mürəkkəb müxtəlifliyini xəritələşdirmək üçün bu texnikadan istifadə etmişdir.
Bununla belə, bu partlayıcı böyümənin altında davamlı problem yatır: qruplaşmanın qeyri-sabitliyi. Tədqiqatçılar hüceyrə növlərini və ya xəstəlik vəziyyətlərini müəyyən etmək üçün hüceyrələri ifadə nümunələri ilə qruplaşdırmağa cəhd etdikdə , eyni verilənlər toplusunu dəfələrlə təhlil etsələr belə, çox vaxt uyğun olmayan nəticələrlə üzləşirlər.
Qeyri-dəqiq qruplaşma normal hüceyrələrin xərçəngli və ya çatışmayan nadir, lakin kritik hüceyrə növləri kimi yanlış təsnif edilməsinə səbəb ola bilər – şərh və terapevtik qərarları təhlükə altına qoyur. Bu “etibarlılıq böhranı” alimləri təhlilləri təkrar etməyə və ya etibarlı fikirlər əldə etmək üçün hesablama baxımından bahalı boru kəmərlərinə etibar etməyə məcbur edir.
İndi Koreyanın Qabaqcıl Elm və Texnologiya İnstitutunun (KAIST) və Əsas Elmlər İnstitutunun (IBS) professoru Kim Jae Kyoungun rəhbərlik etdiyi tədqiqat qrupu həll yolu hazırlayıb: scICE (bir hüceyrəli uyğunsuzluq klasterinin təxminçisi) adlı riyazi çərçivə. Tədqiqat Nature Communications jurnalında dərc olunub .
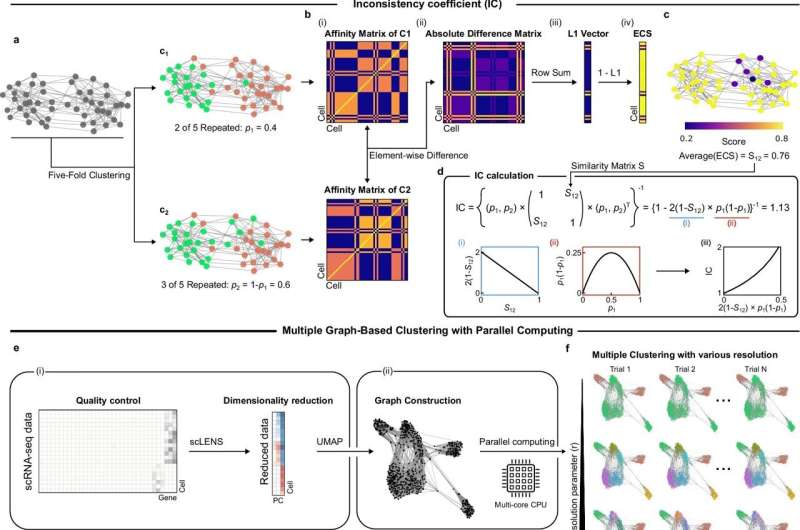
Ənənəvi olaraq, klasterləşmənin etibarlılığı fərdi hüceyrə cütlərinin eyni klasterə təsnif edilib-edilməməsinin təkrar təhlili vasitəsilə konsensus əldə etməklə qiymətləndirilir. Bununla belə, bu yanaşma hesablama tələb edən prosesdir və on minlərlə hüceyrədən ibarət geniş miqyaslı verilənlər topluları üçün uyğun deyil.
Bunun əksinə olaraq, scICE böyük miqyaslı məlumat dəstlərinə tətbiq oluna bilər, çünki o, hesablama tələb edən cüt-cüt qruplaşma prosesini keçmir. Bunun əvəzinə birbaşa hüceyrə təyinatlarının sabitliyini qiymətləndirmək üçün riyazi olaraq müəyyən edilmiş uyğunsuzluq əmsalı (IC) istifadə edir. Bu, alətə yalnız ən sabit və bioloji cəhətdən mənalı klasterləri saxlayaraq etibarsız tapşırıqları səmərəli şəkildə aşkar etməyə və filtrləməyə imkan verir.

Məqalənin (IBS) ilk müəllifi Dr. Kim Hyun izah etdi: “Tək hüceyrəli klasterləşmədə etibarlılıq çoxdan nəzərdən qaçırılıb. sICE nəticələri tez və asanlıqla yoxlamaq üçün yeni yol açır.”
Tədqiqat qrupu beyin, ağciyərlər və qan da daxil olmaqla müxtəlif toxumalardan toplanmış 48 real və simulyasiya edilmiş scRNA-seq verilənlər bazasına tətbiq etməklə SCICE-nin effektivliyini təsdiqlədi. Nəticələr göstərdi ki, mövcud təhlillərin təxminən üçdə ikisi statistik cəhətdən qeyri-sabit və etibarsızdır.
https://googleads.g.doubleclick.net/pagead/ads?gdpr=0&us_privacy=1—&gpp_sid=-1&client=ca-pub-0536483524803400&output=html&h=280&slotname=8188791252&adk=1645945215&adf=2612643799&pi=t.ma~as.8188791252&w=750&abgtt=6&fwrn=4&fwrnh=0&lmt=1751608883&rafmt=1&armr=3&format=750×280&url=https%3A%2F%2Fphys.org%2Fnews%2F2025-07-scientists-tackle-cell-reliability-crisis.html&fwr=0&rpe=1&resp_fmts=3&wgl=1&uach=WyJXaW5kb3dzIiwiMTkuMC4wIiwieDg2IiwiIiwiMTM3LjAuNzE1MS4xMjAiLG51bGwsMCxudWxsLCI2NCIsW1siR29vZ2xlIENocm9tZSIsIjEzNy4wLjcxNTEuMTIwIl0sWyJDaHJvbWl1bSIsIjEzNy4wLjcxNTEuMTIwIl0sWyJOb3QvQSlCcmFuZCIsIjI0LjAuMC4wIl1dLDBd&dt=1751608883748&bpp=3&bdt=134&idt=-M&shv=r20250630&mjsv=m202507020101&ptt=9&saldr=aa&abxe=1&cookie=ID%3Df22668bce9793ae4%3AT%3D1735196613%3ART%3D1751608807%3AS%3DALNI_Mb4Xpwl1SO1AcvqroR6xccDm_sheQ&gpic=UID%3D00000f7c5320f40b%3AT%3D1735196613%3ART%3D1751608807%3AS%3DALNI_Mb1dz_DHiT2yDzXLMaB9CDkQl4XGg&eo_id_str=ID%3D1241933dda87baba%3AT%3D1750839581%3ART%3D1751608807%3AS%3DAA-AfjZwPuiSAour3k16ZA1JtXua&prev_fmts=0x0&nras=1&correlator=4198136257&frm=20&pv=1&rplot=4&u_tz=240&u_his=3&u_h=1080&u_w=1920&u_ah=1032&u_aw=1920&u_cd=24&u_sd=1&dmc=8&adx=448&ady=2470&biw=1905&bih=945&scr_x=0&scr_y=0&eid=31093234%2C95353386%2C95362656%2C95365226%2C31093300%2C95365108%2C95359266%2C95365118%2C95340253%2C95340255&oid=2&pvsid=4419445168433205&tmod=947375100&uas=0&nvt=1&ref=https%3A%2F%2Fphys.org%2F&fc=1920&brdim=0%2C0%2C0%2C0%2C1920%2C0%2C1920%2C1032%2C1920%2C945&vis=1&rsz=%7C%7CpeEbr%7C&abl=CS&pfx=0&fu=128&bc=31&bz=1&td=1&tdf=2&psd=W251bGwsbnVsbCxudWxsLDNd&nt=1&ifi=2&uci=a!2&btvi=1&fsb=1&dtd=65
Eyni zamanda, scICE yüksək dəqiqliyi qoruyarkən tədqiqatçıların vaxtına və hesablama resurslarına qənaət edərək, yalnız az sayda etibarlı nəticələr seçdi.
scICE, bir hüceyrəli məlumatlardan çıxarılan nəticələrə daha yüksək inamı təmin edərək, klasterləşdirmə nəticələrini riyazi olaraq təsdiqləmək üçün bir yol təqdim edir. Bundan əlavə, scICE adi klasterləşdirmə üsulları ilə tez-tez nəzərdən qaçırılan nadir hüceyrə növlərini effektiv şəkildə aşkar etmək qabiliyyəti ilə diqqəti cəlb etmişdir.
Praktikada, scICE öz çərçivəsinə əsaslanan alt qruplaşmadan istifadə edərək, ənənəvi analizlərdə asanlıqla əldən çıxa bilən nadir immun hüceyrələrini etibarlı şəkildə müəyyən etdi.
Müxbir müəllif, professor Kim Jae Kyoung, “scICE tədqiqatçılara etibarlı nəticələrə əsaslanan təqib tədqiqatlarını sürətlə davam etdirməyə kömək edəcək. Ümid edirəm ki, bu, həyat elmləri üzrə etibarlı məlumatların təfsiri üçün standart bir vasitəyə çevriləcək” dedi.
Tədqiqat qrupu sICCE-ni GitHub -da ictimaiyyətə təqdim etdi .
Daha çox məlumat: Hyun Kim və digərləri, scICE: çox klasterli etiket ardıcıllığının qiymətləndirilməsi ilə scRNA-seq məlumatlarının klasterləşmə etibarlılığının və səmərəliliyinin artırılması, Nature Communications (2025). DOI: 10.1038/s41467-025-60702-8
Jurnal məlumatı: Nature Communications
Əsas Elmlər İnstitutu tərəfindən təmin edilmişdir