Alzheimer xəstəliyinin siçan modelində CBD-nin beyin zədələnməsini geri qaytardığı aşkar edildi
İnqrid Fadelli , Medical Xpress tərəfindən
Sadie Harley tərəfindən redaktə edilib , Robert Egan tərəfindən nəzərdən keçirilib
Tercih edilən mənbə kimi əlavə edin
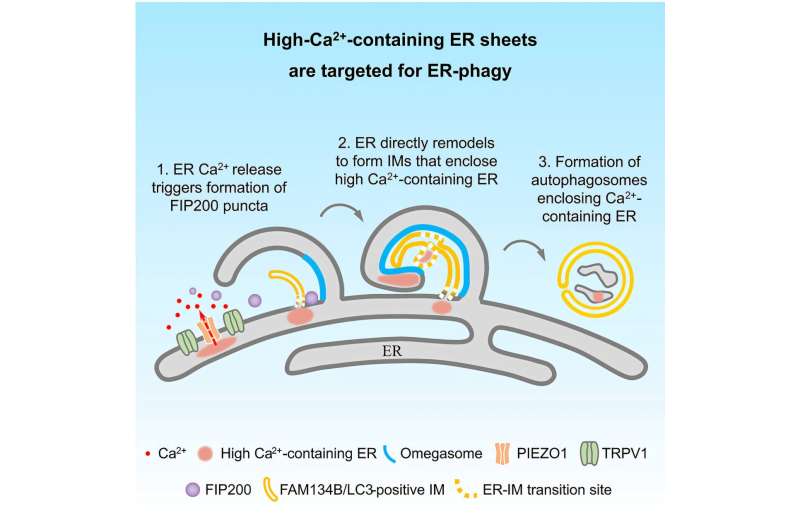
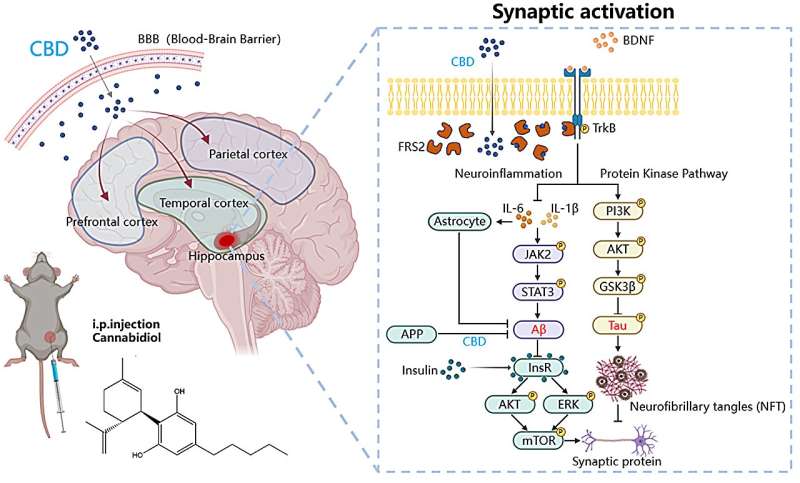
Tədqiqatın sxematik xülasəsi. Diaqram bu işdə aşkar edilmiş CBD-nin neyroprotektiv mexanizmini göstərir. CBD, TrkB-FRS2 siqnal kompleksini sabitləşdirmək üçün molekulyar yapışqan kimi çıxış edərək, adapter zülalı FRS2-yə birbaşa bağlanır. Bu, aşağı axın PI3K/AKT yolunun aktivləşməsini BDNF-dən asılı olmayan şəkildə dəstəkləyir. Bu mexanizm vasitəsilə tək bir CBD müdaxiləsi eyni zamanda Tau hiperfosforlaşmasını yatırır, Aβ çökməsini azaldır, neyroiltihabı yüngülləşdirir, insulin həssaslığını bərpa edir və nəticədə sinaptik arxitekturanı və idrak funksiyasını xilas edir. Müəllif: Liu və digərləri ( Molekulyar Psixiatriya , 2026).
Alzheimer xəstəliyi (AD) mütərəqqi yaddaş itkisi, idrakın azalması və davranış dəyişiklikləri ilə xarakterizə olunan neyrodegenerativ bir xəstəlikdir. AD ilə əlaqəli çatışmazlıqların beyində və sinir hüceyrələri arasında zülalların, xüsusən də tau və β-amiloidin (Aβ) anormal toplanması nəticəsində yarandığı və neyroiltihaba səbəb olduğu və beyin hüceyrələrinin parçalanmasına səbəb ola biləcəyi məlumdur.
Kannabis sativa bitkisindən əldə edilən kannabidiol (CBD) adlı qeyri-psixoaktiv birləşmənin beyin hüceyrələrini zədələnmədən qorumaq üçün perspektivli olduğu bu yaxınlarda aşkar edilmişdir.
Eyforiya hissləri yaradan və istifadəçinin zehni vəziyyətini dəyişdirən sirrdəki birləşmə olan Δ9-tetrahidrokannabinol (THC) ilə müqayisədə CBD daha təhlükəsizdir və buna görə də klinik şəraitdə tətbiqi daha asan ola bilər.
Şençjen Universitetinin, Çin Elmlər Akademiyasının və digər institutların tədqiqatçıları CBD-nin AD-nin siçan modelinə təsirini araşdıran bir araşdırma apardılar.
Molecular Psychiatry jurnalında dərc olunan araşdırmaların nəticələri , CBD-nin təkrar qəbulunun AD-yə bənzər simptomları olan siçanlarda zülalların zərərli yığılmasını necə azalda biləcəyinə, beyin əlaqələrini bərpa edə biləcəyinə və yaddaşı necə yaxşılaşdıra biləcəyinə dair yeni bir fikir təqdim edir.
“Əvvəlki tədqiqatlar göstərib ki, CBD Tau patologiyasını azalda, neyroiltihabı azalda və AD modellərində sinaptik və koqnitiv funksiyanı yaxşılaşdıra bilər”, – məqalənin baş müəllifi Xiubo Du Medical Xpress-ə bildirib.
“Lakin, əsas bir boşluq qalır; CBD-nin molekulyar səviyyədə necə işlədiyini, xüsusən də beyində hansı zülalın təsir etdiyini tam olaraq anlamırıq. Bu bilik olmadan onun effektivliyini izah etmək, optimallaşdırmaq çətindir.”
CBD ilə siçanlarda beyin funksiyasının bərpası
Bu son tədqiqatın ilk məqsədi AD-nin siçan modelində CBD-nin idrakı yaxşılaşdıra və idrak pozğunluqlarını azalda biləcəyini daha da yoxlamaq idi. Eyni zamanda, tədqiqatçılar həmçinin CBD-nin neyroprotektiv faydalarının əsasını təşkil edə biləcək və terapevtik olaraq hədəflənə biləcək molekulyar prosesləri müəyyən etməyə ümid edirdilər.
Du və həmkarları üçqat transgenik AD siçanları kimi tanınan AD-nin siçan modelini araşdırdılar. Bunlar Tau zülal dolaşıqlarının əmələ gəlməsi və Aβ-nin toplanması nəticəsində sinapsları tədricən zədələnən genetik modifikasiya olunmuş siçanlardır. Bu siçanlar AD xəstələrində müşahidə olunanlara bənzər xüsusiyyətlərə malikdirlər, məsələn, yaddaş itkisi və narahatlıq kimi davranışlar.
Əvvəlcə tədqiqatçılar siçanları həftədə altı gün, ümumilikdə 45 gün ərzində CBD ilə müalicə etdilər. Bu müalicə müddətindən sonra onlar siçanların davranışlarını müşahidə etdilər və beyinlərini araşdırdılar.
Maraqlıdır ki, onlar siçanların müalicədən sonra yaddaşının yaxşılaşdığını və narahatlıq səviyyələrinin daha aşağı olduğunu aşkar etdilər. Bundan əlavə, onların beynindəki dendritik onurğalar və sinapsların ümumi quruluşu (yəni neyronlar arasındakı birləşmələr) bərpa olunmuş kimi görünürdü.
“Daha sonra CBD-nin müşahidə etdiyimiz təsirləri necə əldə etdiyinə baxdıq”, – deyə Du bildirib. “Məlum oldu ki, o, neyronların sağ qalması və plastikliyi üçün vacib olan TrkB-PI3K-AKT yolunu aktivləşdirir. Maraqlıdır ki, TrkB-nin kanonik aktivatoru olan beyindən əldə edilən neyrotrofik amil (BDNF) CBD müalicəsindən sonra dəyişməz qalıb. Bu, CBD-nin fərqli bir mexanizmdən istifadə etdiyini göstərir.”
FRS2 proteininin əsas rolu
Du və həmkarları həmçinin termal proteom profilləmə adlanan bir texnikadan istifadə edərək CBD-nin siçan beynində bağlandığı zülalı müəyyən etməyə çalışdılar. Bu, toxumaların və ya hüceyrələrin müəyyən bir birləşmə ilə işlənməsini, müxtəlif temperaturlarda qızdırılmasını, açılan zülalların çıxarılmasını və qalan zülalların təhlil edilməsini əhatə edən laboratoriya yanaşmasıdır.
“İdeya sadədir: kiçik bir molekul bir zülala bağlandıqda, zülal daha sabit olur – sanki əl-ələ tutan iki insanın ayrılması daha çətinləşir”, – deyə Du izah etdi. “Bu ekran vasitəsilə FRS2 namizəd kimi ortaya çıxdı və CBD müalicəsindən sonra artan istilik stabilliyini göstərdi.”
Du və həmkarları daha sonra neyrobioloqlar tərəfindən geniş istifadə edilən müxtəlif üsullardan, o cümlədən flüoresan söndürmə, səth plazmon rezonansı (SPR), biotəbəqə interferometriyası (BLI) və hüceyrə istilik sürüşməsi analizlərindən (CETSA) istifadə edərək tapıntılarını təsdiqləməyə çalışdılar. Bu əlavə testlərin hamısı CBD-nin xüsusi və birbaşa FRS2 adlı bir zülala bağlandığını təsdiqlədi.
“Molekulyar dinamika simulyasiyalarını işlətdiyimiz zaman, tək bir bağlayıcı cibə kilidlənən ənənəvi dərmanlardan fərqli olaraq, CBD-nin FRS2 səthi boyunca dinamik şəkildə paylandığını və nəticədə TrkB-FRS2 protein-zülal interfeysində zənginləşdiyini aşkar etdik”, – deyə Du bildirib.
“Burada, CBD-nin hidroksil qrupu TrkB üzərində spesifik tirozin qalıqları ilə hidrogen rabitələri əmələ gətirir, hidrofob bölgəsi isə FRS2 ilə qarşılıqlı əlaqədə olur və onların əlaqəsini gücləndirən ‘molekulyar yapışqan’ kimi fəaliyyət göstərir və bununla da siqnal kompleksini sabitləşdirir və aşağı axın yolunun aktivləşməsini təmin edir.”
FRS2-nin rolunu daha dərindən araşdırmaq üçün tədqiqatçılar, müəyyən genləri məhv etmək və ya müəyyən zülalların istehsalının qarşısını almaq üçün hüceyrələrə daxil edilə bilən kiçik bir RNT parçası olan shRNA istifadə edərək siçanlarda onun istehsalını blokladılar.
Onlar aşkar etdilər ki, bu zülalın istehsalı azaldıqda, CBD zülalların zərərli yığılmasının qarşısını almaqda, sinapsları qorumaqda və siçanların zehni fəaliyyətini yaxşılaşdırmaqda xeyli az təsirli olur.
“Bu, FRS2-nin CBD-nin neyroprotektiv təsirləri üçün vacib olduğunu təsdiqlədi”, – deyə Du bildirib. “Tapıntılarımızla bağlı ən təəccüblü hesab etdiyim şey, CBD-nin BDNF-ni əvəz etməməsidir – BDNF-nin qurduğu siqnal körpüsünü gücləndirir. Sərt “açar və kilid” cibinə uyğunlaşmaq əvəzinə, TrkB-FRS2 interfeysində molekulyar yapışqan kimi çıxış edir. Bu müşahidə elmi tədqiqatlar və terapevtik müdaxilə üçün mühüm nəticələrə səbəb ola bilər.”
Ümidverici bir terapevtik hədəf
Du və həmkarları tərəfindən toplanan nəticələr, CBD-nin beyində zülalların yığılmasını azalda, iltihabı azalda və sağlam beyin funksiyasını təşviq edə biləcəyi bioloji proseslərə yeni işıq saldı. Bundan əlavə, komanda FRS2 və TrkB kimi zülallar arasındakı qarşılıqlı təsirlərin CBD kimi bu zülallara bağlanan molekullardan istifadə edərək terapevtik olaraq hədəflənə biləcəyini göstərdi.
Du bildirib ki, “Bu terapevtik yanaşma BDNF əsaslı terapiyaların çətinliklərini – zəif stabilliyi, məhdud beyinə nüfuz etmə və tutma riskini aradan qaldırır”.
“Biz CBD-nin davamlı, yumşaq neyroproteksiya təmin etdiyini və təəccüblüdür ki, tək bir müdaxilənin birdən çox patologiyanı: Tau, Aβ, neyroiltihab və sinaptik itkini yaxşılaşdıra biləcəyini aşkar etdik.”
Əgər insanlarda təsdiqlənərsə, komandanın tapıntıları FRS2 və TrkB zülalları arasındakı interfeysi hədəf alan AD üçün yeni müalicələrin inkişafına yol aça bilər. Xüsusilə, bu, CBD-dən daha yaxşı və daha selektiv şəkildə bu zülallara bağlanan yeni dərmanların dizaynına təsir göstərə bilər.
Du dedi: “Məni ən çox həyəcanlandıran şey ‘ liqanddan asılı olmayan aktivləşmə ‘ anlayışıdır . İnkişaf etmiş AD-də neyronlar BDNF istehsal etmək qabiliyyətini itirir. CBD BDNF tələb etmədən TrkB-ni aktivləşdirdiyindən, bu yol hətta sonrakı mərhələlərdə də əlçatan qalır – əksər xəstələrə xəstəliyin əhəmiyyətli dərəcədə irəliləməsindən sonra diaqnoz qoyulduğu üçün vacib bir məqam.”
Gələcəkdə bu son tədqiqat AD və digər neyrodegenerativ xəstəliklərin müalicəsi üçün yeni imkanlar aça bilər. Bu arada, Du və həmkarları müşahidələrini davam etdirməyi və FRS2 və TrkB zülallarını hədəf alan yeni dərmanlar hazırlamağı planlaşdırırlar.
Du dedi: “CBD-nin məhdudiyyətləri var – orta dərəcədə effektivlik və potensial hədəfdən kənar təsirlər. İndi CBD iskelesini yenidən qurmaq üçün struktur yönümlü dizayndan istifadə edirik, FRS2-TrkB interfeysində bağlanmanı gücləndirərkən istənməyən qarşılıqlı təsirləri azaltmaq üçün sterik maneə tətbiq edirik. Məqsədimiz təkmilləşdirilmiş potensiala və selektivliyə malik yeni nəsil molekulyar yapışqanlar hazırlamaqdır.”
Gələcək işlərinin bir hissəsi olaraq, tədqiqatçılar, sporadik AD kimi tanınan ən çox yayılmış AD formasını təqlid edən siçan modelləri üzərində dizayn etdikləri yeni optimallaşdırılmış molekulları sınaqdan keçirməyi planlaşdırırlar. Bu, irsi genetik mutasiyalarla əlaqələndirilə bilməyən və insanlarda AD hallarının 95%-dən çoxunu təşkil etdiyi təxmin edilən AD növüdür.
Du əlavə etdi: “Biz həmçinin bu molekulyar yapışqan strategiyasının digər neyrodegenerativ xəstəliklərə də tətbiq olunub-olunmadığını araşdırırıq”.
“Nəticə etibarilə, biz ‘zülal kompleksi homeostazının yenidən proqramlaşdırılmasını’ yeni bir farmakoloji paradiqma kimi qurmağı hədəfləyirik – patologiyanın təmizlənməsindən kənara çıxaraq funksional bərpaya doğru irəliləyərək, mexaniki olaraq müəyyən edilmiş dərman namizədlərini daha da inkişaf etdirməyə hazır şəkildə.”
Müəllifimiz İnqrid Fadelli tərəfindən sizin üçün yazılmış, Sadie Harley tərəfindən redaktə edilmiş və Robert Egan tərəfindən faktlar yoxlanılmış və nəzərdən keçirilmişdir — bu məqalə diqqətli insan əməyinin nəticəsidir. Müstəqil elmi jurnalistikanı yaşatmaq üçün sizin kimi oxuculara güvənirik. Bu reportaj sizin üçün vacibdirsə, xahiş edirik ianə etməyi düşünün (xüsusilə aylıq). Təşəkkür olaraq reklamsız hesab əldə edəcəksiniz .
Nəşr detalları
Jiantao Liu və digərləri, Alzheimer xəstəliyi patologiyası və koqnitiv pozğunluğun zəiflədilməsində FRS2 qarşılıqlı təsiri vasitəsilə kannabidiol vasitəçiliyi ilə TrkB aktivləşməsinə dair mexaniki anlayışlar, Molekulyar Psixiatriya (2026). DOI: 10.1038/s41380-026-03525-3 .
Jurnal məlumatları: Molekulyar Psixiatriya