Atom səviyyəli simulyasiyalar kritik biomolekulyar mühərrikin arxasındakı fırlanma mexanizmini ortaya qoyur
RIKEN tərəfindən
redaktə edən: Gaby Clark , rəy verən: Robert Egan
Tercih edilən mənbə kimi əlavə edin
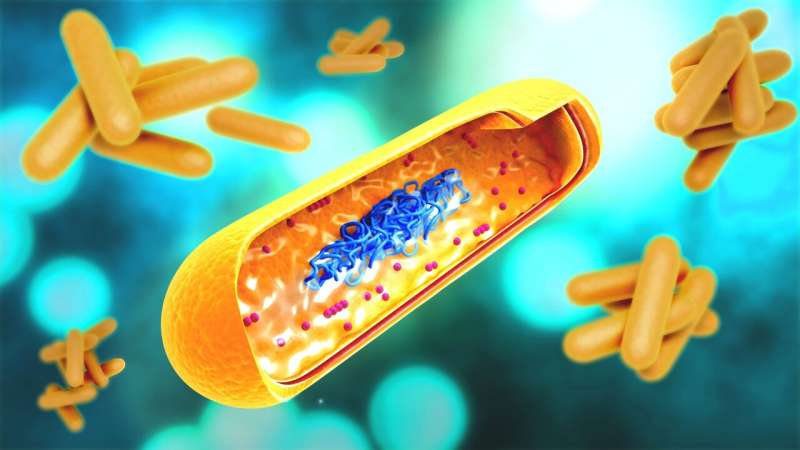
ATP sintazının rotor halqa komponentini göstərən molekulyar model. Molekulyar dinamika tədqiqatında RIKEN tədqiqatçıları F1-ATFaza üçün fırlanma mexanizmini kəşf ediblər. Mənbə: Laguna Design/Science Photo Library
RIKEN biofizikləri tərəfindən aparılan simulyasiyalar əsas hüceyrə mühərrikinin atom səviyyəsində necə işlədiyini aşkar etmişdir. ” Proceedings of the National Academy of Sciences” jurnalında dərc olunan bu tapıntı, hüceyrələrdə mexaniki qüvvənin necə yarandığına dair mühüm məlumatlar verir.
Hüceyrələrimizdəki proseslərin çoxu adenozin trifosfat (ATP) kimi tanınan vacib enerji saxlayan molekul tərəfindən idarə olunur. Tipik bir insan hüceyrəsi işləməsi üçün lazım olan enerjini yaratmaq üçün saniyədə milyonlarla ATF molekulundan istifadə edir.
RIKEN Nəzəri Molekulyar Elm Laboratoriyasından Yuji Sugita deyir: “ATP hüceyrələrdə vacib bir molekuldur. Bir çox motor zülalı kimyəvi enerjini mexaniki işə çevirmək üçün ATF-nin hidrolizindən istifadə edir.”
ATF , əks istiqamətlərdə fırlanan iki molekulyar mühərrikdən, Fo və F1-dən ibarət olan ATPase adlı bir ferment tərəfindən istehsal olunur. Fo-nun sapı protonlar tərəfindən “ döndürüldükdə ” , F1-in ATF molekullarını fırlatmasına imkan verir .
İndi Sugita və onun həmkarları RIKEN-dəki Fugaku superkompüterindən istifadə edərək ətraflı molekulyar simulyasiyalar apararaq F1-ATFazanın fırlanmasını araşdırıblar.
Sugita qeyd edir ki , “F1 – ATFaza ən maraqlı molekulyar mühərriklərdən biridir və struktur və funksional olaraq ən yaxşı öyrənilmişdir. Onun üzərində uzun bir tədqiqat tarixi var.”
Lakin, hesablama məhdudiyyətlərinə görə, əvvəlki molekulyar simulyasiyalar F1-ATFazanı tam şöhrətində modelləşdirməyə imkan vermirdi . Bunun əvəzinə, onlar ya kurslaşdırılmış modellərdən istifadə etməyə, ya da F1-ATFazanın fırlanmasını idarə etmək üçün xarici qüvvə daxil etməyə müraciət etməli idilər .
Sugita və komandası Fuqakudan istifadə edərək bu məhdudiyyəti aradan qaldıra bildilər.
Sugita deyir: “Modelləşdirdiyimiz sistem olduqca mürəkkəbdir , yarım milyondan çox atomdan ibarətdir və biz bu sistemin 64 aralıq strukturunu yaratdıq. Fugaku bizə əvvəlki tədqiqatlarda mümkün olmayan 64 molekulyar dinamika simulyasiyasını paralel olaraq həyata keçirməyə imkan verdi.”
F1 – ATPase, hərəkətsiz komponentə nisbətən 120 dərəcə fırlanan fırlanan elementə malikdir. Bu fırlanma iki mərhələdə baş verir: biri 80 dərəcə, digəri isə 40 dərəcə. Komanda bu tədqiqatda 80 dərəcəlik addımı təhlil etdi.
Onlar bu fırlanma üçün yeni bir mexanizm kəşf etdilər və bunun F1 -ATFazasının stasionar hissəsinin deformasiyası və ardınca fırlanan hissəyə təsir edən itələyici qüvvə ilə idarə olunduğunu aşkar etdilər.
Sugita deyir ki, “80 dərəcəlik fırlanmanı əvvəllər nəzərdən keçirilməmiş bu təhrif-itələmə mexanizmi baxımından izah edə bilərik”.
Komandanın fırlanma mexanizmi, krio-elektron mikroskopiyası və tək molekullu spektroskopiya istifadə edilərək əldə edilən molekulyar strukturlar da daxil olmaqla, F1-ATFaza ilə bağlı eksperimental müşahidələrlə uyğundur .
Komanda indi eyni yanaşmanı F1- ATPase -nin ikinci, 40 dərəcəlik fırlanmasına tətbiq etmək niyyətindədir .