Bakterial biofilm müdafiəsinə yeni perspektiv üçün klassik texnikanın yenidən tətbiqi
Lori Dajose, Kaliforniya Texnologiya İnstitutu
Lisa Lock tərəfindən redaktə edilmiş , Robert Eqan tərəfindən nəzərdən keçirilmişdir
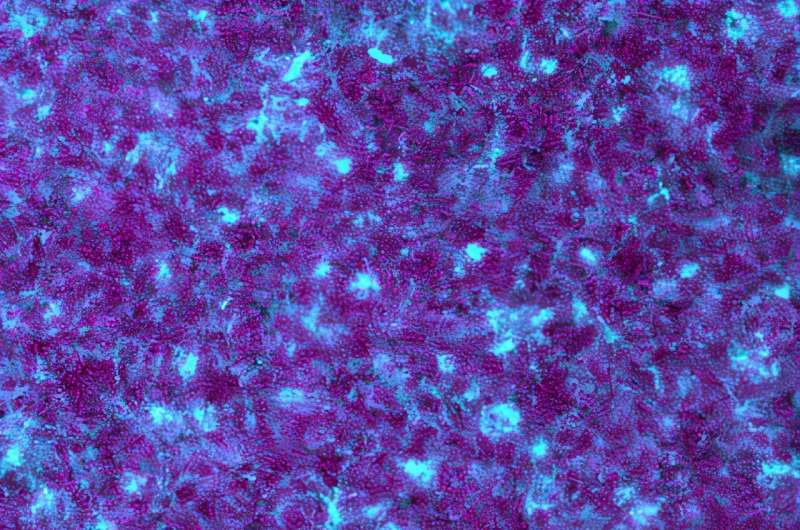
Redaktorların qeydləriMagenta ilə etiketlənmiş bakteriyalar, yapışqan hüceyrədənkənar matrislə (mavi) birləşən kütləvi biofilm icmasını təşkil edir. Kredit: G. Squyres
Caltech tədqiqatçıları biofilmləri, çox vaxt antibiotiklərə dözümlü infeksiyalardan məsul olan milyonlarla hüceyrədən ibarət yapışqan kütlələri təşkil edən fərdi hüceyrələrin formalaşması və böyüməsini təsvir etmək üçün klassik bir texnikanı yenidən tətbiq etdilər. Metod, xroniki infeksiyalar kontekstində onlarla mübarizə aparmağa kömək etmək potensialına malik olan anlayışlar təklif edərək, biofilmlərin necə davrandığına dair uzun müddətdir davam edən suallara cavab verməyə kömək edəcək.
Tədqiqat Biologiya və Geobiologiya üzrə Qordon M. Binder/Amgen Professoru və Merkin İnstitutunun professoru Dianne Newmanın laboratoriyasında aparılıb və doktoranturadan sonrakı alim Corciya Squyres rəhbərlik edib. Əsəri təsvir edən məqalə Proceedings of the National Academy of Sciences jurnalında dərc olunub .
Bütövlükdə biofilmlər ayrı-ayrı hüceyrələrdə olmayan xüsusiyyətlərə malikdir. Buraya müdafiə matrisi kimi onları antibiotiklərdən qoruyan qrup davranışları daxildir. Squyres və Newman biofilmdəki hüceyrələrin bu müdafiəni qurmaq üçün necə birlikdə işlədiyini anlamaq istədi.
Bunun üçün tədqiqatçılar ilk növbədə bütün biofilm hüceyrələrinin davranışını bir anda təsvir edə və izləyə bilməlidirlər. Bioloji görüntüləmə tez-tez flüoresan zülallarla aparılır, lakin onların işləməsi üçün oksigen tələb olunur. Əsas odur ki, biofilmlərin daxili nüvələri çox vaxt oksigendən məhrumdur, yəni hüceyrələri flüoresanla etiketləmək üçün adi üsullar işləmir.
Yeni araşdırmada Squyres ucuz, toksik olmayan boyadan istifadə edərək hüceyrələrin özləri deyil, hüceyrələrin böyüdüyü mühiti etiketləmək üçün flüoresan texnikanı yenidən tətbiq etdi; boya parlaq fonda hüceyrələri qaranlıq etdi. Bu üsul hətta biofilm nüvəsində də işləyir və biofilmlərin yüksək qətnamə ilə təsvir oluna biləcəyi vaxtı artırır. Bu üsulu ayrı-ayrı hüceyrələrin davranışını aşkar etmək üçün bir alqoritmlə birləşdirərək, Squyres bir çox gün ərzində biofilmin böyüməsini və hüceyrə dinamikasını izləyə bildi.Oyna
00:0000:03SəssizParametrlərPIPTam ekrana daxil olun
OynaBiofilm nüvəsinə oksigen daxil edilməsi hüceyrə lizisinə səbəb olur. Kredit: Milli Elmlər Akademiyasının Materialları (2025). DOI: 10.1073/pnas.2514210122
Komanda, tez-tez infeksiyalara cavabdeh olan, tez-tez tədqiq edilən patogen olan Pseudomonas aeruginosa-dan istifadə etdi, lakin bu texnika biofilmlər əmələ gətirən istənilən bakteriya növünə tətbiq oluna bilərdi.
https://googleads.g.doubleclick.net/pagead/ads?gdpr=0&us_privacy=1—&gpp_sid=-1&client=ca-pub-0536483524803400&output=html&h=280&slotname=8188791252&adk=1645945215&adf=308666314&pi=t.ma~as.8188791252&w=750&fwrn=4&fwrnh=0&lmt=1761905794&rafmt=1&armr=3&format=750×280&url=https%3A%2F%2Fphys.org%2Fnews%2F2025-10-reintroducing-classic-technique-perspective-bacterial.html&fwr=0&rpe=1&resp_fmts=3&wgl=1&aieuf=1&aicrs=1&uach=WyJXaW5kb3dzIiwiMTkuMC4wIiwieDg2IiwiIiwiMTQxLjAuNzM5MC41NSIsbnVsbCwwLG51bGwsIjY0IixbWyJHb29nbGUgQ2hyb21lIiwiMTQxLjAuNzM5MC41NSJdLFsiTm90P0FfQnJhbmQiLCI4LjAuMC4wIl0sWyJDaHJvbWl1bSIsIjE0MS4wLjczOTAuNTUiXV0sMF0.&abgtt=6&dt=1761905794493&bpp=1&bdt=163&idt=26&shv=r20251029&mjsv=m202510290101&ptt=9&saldr=aa&abxe=1&cookie=ID%3Df22668bce9793ae4%3AT%3D1735196613%3ART%3D1761905614%3AS%3DALNI_Mb4Xpwl1SO1AcvqroR6xccDm_sheQ&gpic=UID%3D00000f7c5320f40b%3AT%3D1735196613%3ART%3D1761905614%3AS%3DALNI_Mb1dz_DHiT2yDzXLMaB9CDkQl4XGg&eo_id_str=ID%3D1241933dda87baba%3AT%3D1750839581%3ART%3D1761905614%3AS%3DAA-AfjZwPuiSAour3k16ZA1JtXua&prev_fmts=0x0&nras=1&correlator=3375285478279&frm=20&pv=1&rplot=4&u_tz=240&u_his=4&u_h=1080&u_w=1920&u_ah=1032&u_aw=1920&u_cd=24&u_sd=1&dmc=8&adx=448&ady=2407&biw=1905&bih=945&scr_x=0&scr_y=0&eid=31095438%2C31095509%2C31095510%2C31095513%2C31095515%2C31095564%2C31095567%2C95375933%2C95376113%2C95376297%2C31095556%2C95344791&oid=2&pvsid=5261747952967913&tmod=1941919895&uas=0&nvt=1&ref=https%3A%2F%2Fphys.org%2Fpage2.html&fc=1920&brdim=0%2C0%2C0%2C0%2C1920%2C0%2C1920%2C1032%2C1920%2C945&vis=1&rsz=%7C%7CpeEbr%7C&abl=CS&pfx=0&fu=128&bc=31&plas=596x742_l%7C596x742_r&bz=1&td=1&tdf=2&psd=W251bGwsbnVsbCxudWxsLDNd&nt=1&ifi=2&uci=a!2&btvi=1&fsb=1&dtd=213
“Gürcüstanın gördüyü işlər bir çox səviyyələrdə texniki cəhətdən çətin idi və böyük bir nailiyyətdir” dedi Nyuman. “Ancaq texnikadan daha çox, məni heyran edən onun onunla nə edəcəyinə dair baxışıdır. Bakterial biofilmlərin unikal xüsusiyyətlərindən istifadə edərək, o, inkişaf və hüceyrə biologiyasında yeni sərhədlər açan suallar verir .”
Yeni texnika ilə Squyres biofilmin necə inkişaf etdiyi ilə bağlı açıq suala cavab verdi. Biofilmdəki ayrı-ayrı hüceyrələr DNT-ni ehtiva edən hüceyrədənkənar matris adlanan yapışqan maddə ilə əhatə olunmuşdur . Bu hüceyrədənkənar DNT və ya eDNA, hüceyrələr öləndə və lizis adlanan prosesdə partlayanda matrisə buraxılır. Bu eDNA biofilmin əsas komponentidir, hüceyrələrin bir-birinə yapışmasına kömək edir, ona struktur sabitlik verir və həmçinin biofilmin inkişafı üçün lazım olan müəyyən metabolitləri saxlayır.
Bəzi antibiotiklər də eDNT-də ilişib qalır ki, bu da onların nəzərdə tutulan hüceyrə hədəflərinə çatmasına mane olur. Hüceyrələrin öldüyü zaman eDNT-nin sərbəst buraxıldığını nəzərə alsaq, biofilmdəki müəyyən hüceyrələr matrisdə davamlı eDNA tədarükünü saxlamaq üçün effektiv şəkildə özlərini qurban verirlər.
Bu qurbanlıq hüceyrələrin biofilmdə necə seçildiyini anlamaq üçün Squyres biofilmdə hansı hüceyrələrin lizisə məruz qaldığını vizuallaşdırmaq və onların daha böyük strukturda hər hansı xüsusi mövqedə olub-olmadığını müşahidə etmək istəyirdi. O, hər 10.000 hüceyrədən 1-nin saatda parçalandığını və bu hüceyrələrin biofilm içərisində karbon və oksigen kimi qida maddələrinin qradiyenti ilə formalaşan xüsusi mövqelərdə yerləşdiyini kəşf etdi. Bu lizis hadisələrinin xəritəsini çəkərək, o, biofilmin eDNT matrisinin şəklini necə aldığını anlaya bildi.
Squyres deyir: ” Biofilmlərdə antibiotik tolerantlığı ayrı-ayrı hüceyrələr tərəfindən əlaqələndirilir və ümid edirəm ki, bu iş onların davranışlarını necə öyrənmək üçün yeni bir çərçivə verir”.
Ətraflı məlumat: Georgia R. Squyres və digərləri, Pseudomonas aeruginosabiofilms matrisində eDNT-nin tək hüceyrəli lizis nümunələri morfogenezi, Milli Elmlər Akademiyasının əsərləri (2025). DOI: 10.1073/pnas.2514210122
Jurnal məlumatı: Milli Elmlər Akademiyasının Materialları
Kaliforniya Texnologiya İnstitutu tərəfindən təmin edilmişdir