Bir kimi fəaliyyət göstərməyən ferment: NUDT5 DNT tikinti blokunun istehsalını katalizlə deyil, struktur vasitəsilə idarə edir
Avstriya Elmlər Akademiyasının CeMM Molekulyar Tibb Tədqiqat Mərkəzi tərəfindən
Sadie Harley tərəfindən redaktə edilmiş , Robert Eqan tərəfindən nəzərdən keçirilmişdir
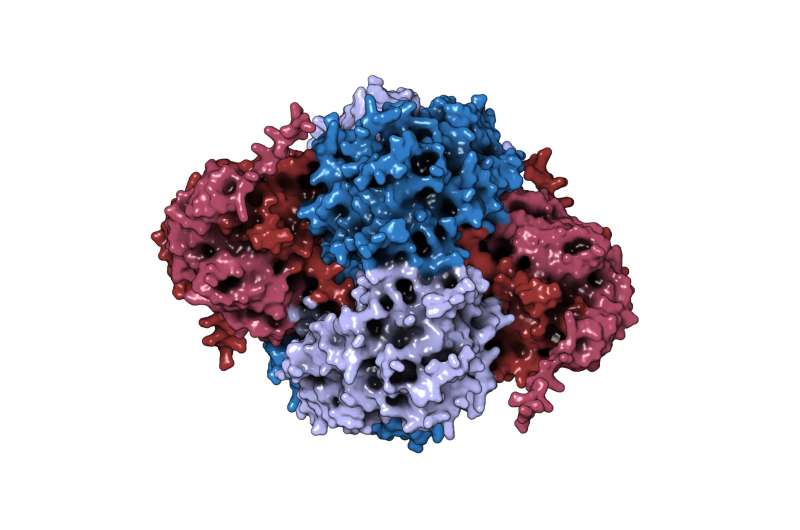
Redaktorların qeydləriNUDT5 dimerləri (qırmızı) və PPAT tetrameri (mavi) arasında alfafold qarşılıqlı əlaqə proqnozu. Kredit: Tuan-Anh Nguyen
Hər bir hüceyrənin içərisində incə tənzimlənmiş metabolik şəbəkə əsas molekulların nə vaxt qurulacağını, təkrar emal ediləcəyini və ya istehsalını dayandıracağını müəyyən edir. Bu şəbəkənin mərkəzi hissəsi DNT, RNT və amin turşularının sintezi üçün həyati vacib kimyəvi vahidləri təmin edən bir proses olan folat metabolizmidir.
Bu sistem pozulduqda – məsələn, genetik mutasiyalar və ya pəhrizdə folatın olmaması – nəticələr inkişaf pozğunluqlarından xərçəngə qədər dəyişə bilər.
İndi Avstriya Elmlər Akademiyasının Molekulyar Təbabət üzrə Tədqiqat Mərkəzi olan CeMM-dən olan tədqiqatçılar Oksford Universitetinin əməkdaşları ilə birlikdə bu metabolik balansda gözlənilməz oyunçunu müəyyən ediblər: NUDT5 fermenti.
Elmdə nəşr olunan araşdırma göstərir ki , NUDT5 purin istehsalını dayandırmağa kömək edir – DNT-nin tikinti bloklarını yaradan kimyəvi yolu – lakin bunu onun fermentativ fəaliyyətindən istifadə etmədən edir. Bunun əvəzinə, zülal, purin səviyyələri artıq yüksək olduqda, əsas biosintetik addımı fiziki olaraq məhdudlaşdıran bir növ molekulyar iskele rolunu oynayır.
Köhnə ferment üçün yeni rol
Purinlər, hüceyrələrin DNT və RNT yaratmaq və enerji saxlamaq üçün istifadə etdiyi vacib molekullardır. Onlar mövcud materialdan təkrar emal edilə bilər və ya sıfırdan de novo yolu deyilən yolla istehsal oluna bilər – bu, ciddi şəkildə idarə edilməli olan enerji tutumlu bir prosesdir.
Tədqiqat zamanı tədqiqatçılar bu nəzarət mexanizmini folat siklinin mühüm fermenti olan MTHFD1 genində mutasiyaları olan hüceyrələri tədqiq edərək araşdırdılar. Folat metabolizması purin sintezi üçün lazım olan bir karbon vahidlərini təmin edir və bu yoldakı qüsurlar nadir genetik xəstəliklərə səbəb olur və xərçəng riskinə təsir göstərir.
Genetik skrininq, metabolomika və kimyəvi biologiyanın birləşməsindən istifadə edən komanda, NUDT5 zülalının purin sintezinin ilk addımını kataliz edən başqa bir ferment olan PPAT ilə qarşılıqlı əlaqədə olduğunu aşkar etdi. Purin səviyyələri yüksəldikdə, NUDT5 PPAT-a bağlanır və çox güman ki, onu qeyri-aktiv formada kilidləyir – hüceyrəyə daha çox purin istehsalını dayandırmağı effektiv şəkildə bildirir.
Təəccüblüdür ki, NUDT5-in bu funksiyası nukleotid törəmələrini parçalayan məlum fermentativ fəaliyyətinə etibar etmir. Hətta onun katalitik yeri kimyəvi cəhətdən bloklandıqda və ya genetik cəhətdən əlil olduqda belə, protein purin sintezini tənzimləməyə davam edirdi. Yalnız NUDT5 tamamilə çıxarıldıqda – ya genetik nokaut, ya da onu seçici şəkildə pozan yeni inkişaf etmiş bir molekul – hüceyrələr bu nəzarət mexanizmini itirdi.Daha çox kəşf edin
Elm
Elmlər
STEM öyrənən oyuncaqlar
Elmi jurnallara abunə
Elm öyrənmə kursları
İqlim dəyişikliyi tədqiqatı
Biotexnologiya hesabatları
Zülal
Fizika təcrübə dəstləri
Astronomiya məqalələri
Tibbi təsirləri olan metabolik nəzarət
Kəşf hüceyrələrin metabolik mühitdəki dəyişiklikləri necə hiss etdiyi və onlara necə reaksiya verdiyinə yeni işıq salır.
CeMM-in baş tədqiqatçısı və tədqiqatın baş müəllifi Stefan Kubicek deyir: “NUDT5 uzun müddətdir metabolitləri hidroliz edən ferment kimi təsnif edilmişdir”.
“Ancaq bizim işimiz tamamilə fərqli bir rolu ortaya qoyur – o, hüceyrənin purinlər istehsal edib-etmədiyini müəyyən edən struktur tənzimləyici kimi çıxış edir.”
Bu mexanizm bəzi hüceyrələrin bəzi xərçəng dərmanlarına niyə müqavimət göstərdiyini də izah edə bilər. Tədqiqatın birinci müəllifi Tuan-Anh Nguyen izah edir: “6-tioquanin kimi bir çox kemoterapiya purin molekullarını təqlid edərək və DNT sintezini bloklayaraq işləyir”.
“Ancaq biz NUDT5-PPAT funksional qarşılıqlı əlaqəsi olmayan hüceyrələrin bu müalicələrə daha az həssas olduğunu, NUDT5-dəki mutasiyaların şişlərdə dərman müqavimətinə kömək edə biləcəyini irəli sürdük.”
NUDT5-in xərçəng dərmanlarına həssaslığın idarə edilməsində əsas rolu eyni zamanda Science jurnalının eyni sayında dərc olunan Ralph DeBerardinis laboratoriyasının oxşar tapıntıları ilə də dəstəklənir .
Bundan əlavə, tədqiqat fol turşusu mübadiləsi, purin sintezi və immun və nevroloji inkişafa təsir edən nadir bir genetik xəstəlik olan MTHFD1 çatışmazlığının səbəb olduğu xəstəliklər arasındakı nöqtələri birləşdirir.
“Folat və purin yolları bir-biri ilə sıx əlaqəli olduğundan, bu tənzimləyici şəbəkəni başa düşmək nəticədə yeni terapevtik yanaşmalar haqqında məlumat verə bilər” deyə tədqiqatın birinci müəllifi Jung-Ming George Lin əlavə edir.
Kilian Huberin Oksforddakı laboratoriyasındakı əməkdaşlar həmçinin hüceyrələrdən NUDT5-i seçici şəkildə aradan qaldıra bilən dNUDT5 adlı kimyəvi deqradator hazırladılar. Bu alət alimlərə yolu daha ətraflı öyrənməyə imkan verəcək və sağlam hüceyrələri kemoterapinin yan təsirlərindən qorumaq üçün gələcək imkanlar təklif edə bilər.
“Bizim tapıntılarımız vurğulayır ki, fermentlər təkcə katalizlədikləri kimyəvi reaksiyalar vasitəsilə deyil, həm də strukturları vasitəsilə hərəkət edə bilirlər” deyə Kubiçek yekunlaşdırır. “Bəzən, mühüm fərqi yaradan zülalın fiziki varlığıdır.”
Daha çox məlumat: Jung-Ming G. Lin et al, Nudix hidrolaza 5-in purin de novo sintezinin repressiyasında qeyri-enzimatik rolu, Elm (2025). DOI: 10.1126/science.adv4257 . www.science.org/doi/10.1126/science.adv4257
Jurnal məlumatı: Elm
Avstriya Elmlər Akademiyasının Molekulyar Tibb üzrə CeMM Araşdırma Mərkəzi tərəfindən təmin edilmişdir