DNT təmir zülalının gözlənilməz quruluşu yeni xərçəng müalicələrinə səbəb ola bilər
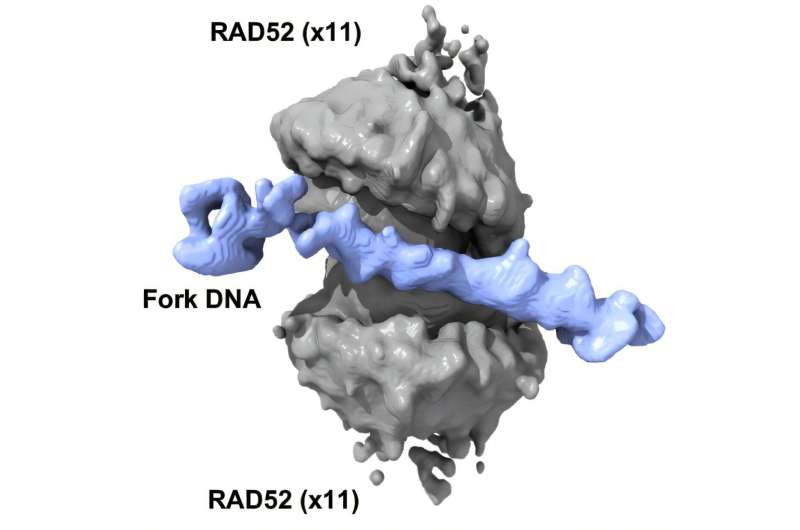
Ayova Universitetinin rəhbərlik etdiyi bir araşdırma, bölünən hüceyrələrdə replikasiya edən DNT-ni bağlayan və qoruyan RAD52 DNT təmir zülalının qəbul etdiyi gözlənilməz quruluşu aşkar etdi. RAD52-DNT kompleksinin bu yeni struktur və mexaniki anlayışı tədqiqatçılara yeni xərçəng əleyhinə dərmanlar hazırlamağa kömək edə bilər.
Tədqiqat Nature jurnalında dərc olunub .
UI Carver Tibb Kollecinin biokimya və molekulyar biologiya professoru və yeni tədqiqatın baş müəllifi Maria Spies, Ph.D., “RAD52, DNT təmiri çatışmazlığı olan xərçənglərin, o cümlədən döş və yumurtalıqların xərçəngi və bəzi glioblastomaların müalicəsi üçün arzu edilən bir dərman hədəfidir” dedi.
“Bu zülal yeni anti-xərçəng dərmanları üçün cəlbedici bir hədəfdir, çünki sağlam insan hüceyrələrində əvəzolunmaz olsa da, RAD52 BRCA1 və BRCA2 genlərində qüsurları olanlar kimi DNT təmir funksiyasında çatışmazlıq olan xərçəng hüceyrələrinin yaşaması üçün vacib olur.”
DNT təmiri çatışmazlığı olan xərçənglər, DNT təmiri üçün ehtiyat yollar təmin etmək üçün digər zülallardan asılıdır ki, bu da xərçəng hüceyrələrinin sürətlə çoxalmasına və DNT zədələnməsinə baxmayaraq sağ qalmasına imkan verir. RAD52 bu zülallardan biridir. Bu o deməkdir ki, RAD52-ni bloklayan və işləməsinə mane olan molekullar bu növ xərçəngin müalicəsi üçün faydalı ola bilər.
Artıq sübut edilmişdir ki, RAD52 inhibitorları xərçəng hüceyrələrini selektiv şəkildə öldürə bilər və radiasiya və kimyaterapiya ilə bağlı toksikliyi minimuma endirir. Bu qabiliyyət hazırda klinik istifadədə olan PARP (poli-ADP-riboza polimeraza) inhibitorları adlanan BRCA1/2 çatışmazlığı olan xərçəngləri hədəf almaq üçün təsdiqlənmiş ilk dərmanların fəaliyyətinə bənzəyir. PARP inhibitoru olaparib ilə müalicə olunan xəstələrin demək olar ki, 15%-i beş ildən çox xəstəlikdən azad olsa da, bir çoxunda ilk il ərzində müqavimət inkişaf edir.
Spies deyir: “RAD52-nin hədəflənməsi (PARP inhibisyonundan asılı olmayaraq və ya onunla birlikdə) mövcud müalicələrin repertuarını artıracaq”. “Lakin, xərçəng hüceyrələrində RAD52-ni inhibə edəcək dərmanlar hazırlamaq üçün əvvəlcə RAD52-nin molekulyar, struktur və hüceyrə səviyyəsində necə işlədiyini başa düşməliyik.”
https://googleads.g.doubleclick.net/pagead/ads?client=ca-pub-0536483524803400&output=html&h=188&slotname=8188791252&adk=1687169288&adf=4054963813&pi=t.ma~as.8188791252&w=750&abgtt=6&fwrn=4&lmt=1743655921&rafmt=11&format=750×188&url=https%3A%2F%2Fphys.org%2Fnews%2F2025-04-dna-protein-unexpected-cancer-treatments.html&wgl=1&uach=WyJXaW5kb3dzIiwiMTkuMC4wIiwieDg2IiwiIiwiMTM0LjAuNjk5OC4xNzgiLG51bGwsMCxudWxsLCI2NCIsW1siQ2hyb21pdW0iLCIxMzQuMC42OTk4LjE3OCJdLFsiTm90OkEtQnJhbmQiLCIyNC4wLjAuMCJdLFsiR29vZ2xlIENocm9tZSIsIjEzNC4wLjY5OTguMTc4Il1dLDBd&dt=1743655920946&bpp=1&bdt=103&idt=130&shv=r20250401&mjsv=m202503310101&ptt=9&saldr=aa&abxe=1&cookie=ID%3Df22668bce9793ae4%3AT%3D1735196613%3ART%3D1743655898%3AS%3DALNI_Mb4Xpwl1SO1AcvqroR6xccDm_sheQ&gpic=UID%3D00000f7c5320f40b%3AT%3D1735196613%3ART%3D1743655898%3AS%3DALNI_Mb1dz_DHiT2yDzXLMaB9CDkQl4XGg&eo_id_str=ID%3Dcdf7f2f01784f52d%3AT%3D1735196613%3ART%3D1743655898%3AS%3DAA-Afjb8kbeupLLyQ0QHQmZxpM4v&prev_fmts=0x0&nras=1&correlator=1965239177121&frm=20&pv=1&rplot=4&u_tz=240&u_his=3&u_h=1080&u_w=1920&u_ah=1032&u_aw=1920&u_cd=24&u_sd=1&dmc=8&adx=448&ady=2141&biw=1905&bih=945&scr_x=0&scr_y=0&eid=95355973%2C95355975%2C95344788%2C95354563%2C95356499%2C95356505%2C31090357%2C95356787%2C95356928&oid=2&pvsid=1542340864050600&tmod=975136302&uas=0&nvt=1&ref=https%3A%2F%2Fphys.org%2F&fc=1920&brdim=0%2C0%2C0%2C0%2C1920%2C0%2C1920%2C1032%2C1920%2C945&vis=1&rsz=%7C%7CpeEbr%7C&abl=CS&pfx=0&fu=128&bc=31&bz=1&td=1&tdf=2&psd=W251bGwsbnVsbCxudWxsLDNd&nt=1&ifi=2&uci=a!2&btvi=1&fsb=1&dtd=135
Yeni forma dərman müalicəsi üçün mümkün hədəfləri ortaya qoyur
RAD52-nin normal insan hüceyrələrində əvəzsiz görünməsi, lakin qüsurlu DNT təmiri yaşayan xərçəng hüceyrələrinin yaşaması üçün vacib olması həm üstünlük, həm də çətinlik yaradır. Üstünlük ondan ibarətdir ki, RAD52-nin inhibə edilməsi xəstənin sağlam hüceyrələrinə minimal mənfi təsir göstərərək xərçəng hüceyrələrini öldürməlidir. Çətinlik RAD52-nin hansı funksiya və xüsusiyyətlərinin hədəf alınmalı olduğunu tapmaqdır.
Yeni araşdırmada Spies və onun UI komandası Romada (İtaliya) Istituto Superiore di Sanità-da molekulyar tibb professoru, Ph.D.Pietro Pichierri və Ph.D.M.Ashley Spies ilə əməkdaşlıq edərək, UI Əczaçılıq Kollecində dərman kəşfi və eksperimental terapevtika professoru, onlara RAD funksiyalı məlumatları kəşf etməyə kömək edə bilər25 bu proteini inhibə etmək üçün yeni, xüsusi yollar.
İkili halqa quruluşu DNT-ni qoruyur
Spies və Pichierri əvvəllər RAD52-nin dayanmış DNT replikasiya çəngəllərinin qorunmasında vacib olduğunu kəşf etmişdilər. Onların işi RAD52-nin bu yeni funksiyasının xərçəng hüceyrələrinin sağ qalmasını asanlaşdırdığını irəli sürdü.
Yeni araşdırmada Spies komandası kriogen elektron mikroskopiyadan (CryoEM) istifadə edərək RAD52 zülallarının hər biri 11 nüsxə protein ehtiva edən RAD52-nin iki halqasından ibarət gözlənilməz makaraya bənzər bir quruluş meydana gətirdiyini göstərmək üçün “DNT replikasiya çəngəli”nin hər üç qolunu birləşdirərək strukturu yenidən təşkil etmək və onu pozmaqdan qoruyur.
Bu təsviri əldə etmək üçün komanda dayanmış DNT replikasiya çəngəlinə bənzəyən DNT substratı yaratdı. Substrat hər üç DNT qolu ilə iki halqanı bir araya gətirərək RAD52 kompleksini yerində düzəldir. Həm tək, həm də cüt zəncirli DNT xüsusiyyətləri RAD52 ilə qarşılıqlı əlaqədə olur və strukturu yerində saxlayır, komandaya bütün zülal-DNT kompleksinin ətraflı 3D strukturunu əldə etməyə imkan verir.
Spies laboratoriyasında qurulmuş xüsusi mikroskoplardan istifadə edərək, tədqiqatçılar həmçinin RAD52-DNT əməliyyatlarını tək molekul səviyyəsində izləyə bildilər və çəngəlin qorunmasının dinamik zülal-DNT qarşılıqlı əlaqəsi vasitəsilə baş verdiyini ortaya qoydular.
Spies deyir: “Tək halqa quruluşu əvvəllər müşahidə edilmiş olsa da, bu, gözlənilməz bir şey edən DNT-də iki halqanın birlikdə göründüyü ilk quruluşdur” dedi. “Bu yeni struktur gələcək dərman kəşfi üçün zülalın hansı mühüm sahələrinin hədəf alına biləcəyinə dair ipuçları verir.”
Gündəlik anlayışlar üçün Phys.org-a etibar edən 100.000-dən çox abunəçi ilə elm, texnologiya və kosmosda ən son yenilikləri kəşf edin . Pulsuz xəbər bülleteni üçün qeydiyyatdan keçin və mühüm nailiyyətlər, yeniliklər və tədqiqatlar haqqında gündəlik və ya həftəlik yeniləmələr əldə edin .Abunə ol
Yeni xərçəng dərmanları yaratmaq üçün RAD52-nin hədəflənməsi
Spies komandası artıq RAD52-ni bağlayan və maneə törədən kiçik molekullara malikdir, lakin bu molekulları sınaqdan keçirilə bilən dərmanlara çevirmək üçün onları daha effektiv və daha spesifik etmək üçün daha da təkmilləşdirilməli və dəyişdirilməlidir.
Spies laboratoriyasının struktur və biofiziki işinin nəticələri M. Ashley Spies tərəfindən hesablama tədqiqatları və Romadakı Pichierri qrupu tərəfindən hüceyrə əsaslı və super rezolyusiyaya malik görüntüləmə ilə tamamlandı. Birlikdə, laboratoriyaların səyləri iki halqalı RAD52 arxitekturasının DNT replikasiya qapıçısı rolunu oynama qabiliyyəti və xərçəng hüceyrələrinin sağ qalması baxımından əhəmiyyətini ortaya qoydu.
Spies deyir: “Bu iş və bu araşdırmada əldə etdiyimiz struktur-fəaliyyət biliklərimiz RAD52 fəaliyyətini və tənzimləməsini anlamaq üçün gələcək işi qurur və onun qarşısını almaq üçün yeni hədəflər təklif edir”. “Ümid edirik ki, bu məlumat bizə bu zülalın yeni inhibitorlarını inkişaf etdirməyə və RAD52 potensialını xərçəng əleyhinə dərman hədəfi kimi istifadə etməyə kömək edəcək .”
Maria Spies, Pichierri və Ashley Spies ilə yanaşı, tədqiqat qrupuna həm də aparıcı müəlliflər Masayoshi Honda, Ph.D. və Mortezaali (Əli) Razzaghi, Ph.D., hər ikisi Spies UI laboratoriyasının tədqiqatçılarıdır. Bundan əlavə, Spies RAD52-nin struktur tədqiqatlarına başlamaqda göstərdikləri köməyə görə UI Protein və Crystallography Core-un hazırkı və keçmiş direktorları Ph.D. Nick Schnicker və Ph.D. Lokesh Qakharın təcrübəsinə borcludur.
Daha çox məlumat: Maria Spies, RAD52 ikiqat halqalı çəngəllərin çevrilməsini məhdudlaşdıran replikasiya çəngəllərini yenidən modelləşdirir, Təbiət (2025). DOI: 10.1038/s41586-025-08753-1 . www.nature.com/articles/s41586-025-08753-1
Jurnal məlumatı: Təbiət
Ayova Universiteti tərəfindən təmin edilmişdir