Hüceyrə yaddaşı açma/söndürmə açarından daha çox sönük siferblat kimi fəaliyyət göstərə bilər
Jennifer Chu, Massaçusets Texnologiya İnstitutu
Lisa Lock tərəfindən redaktə edilmiş , Robert Eqan tərəfindən nəzərdən keçirilmişdir
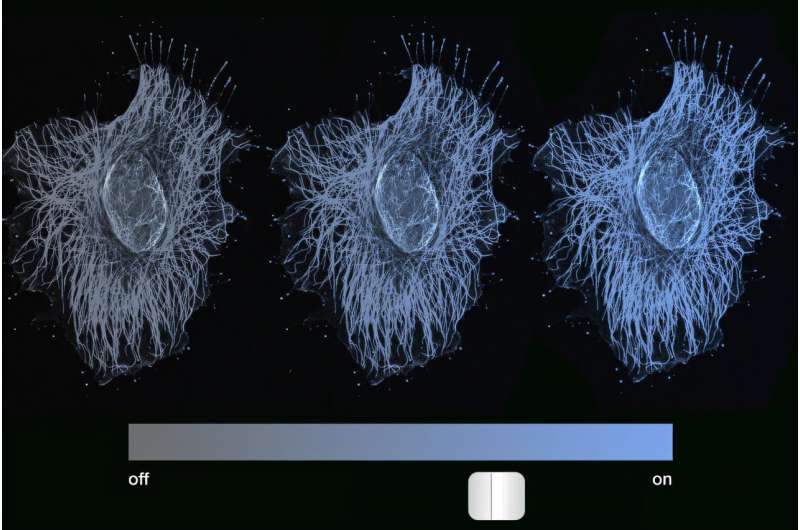
Redaktorların qeydləriƏnənəvi olaraq, elm adamları epigenetik yaddaşın genləri “on” və ya “off” – ya tam aktivləşdirilmiş, ya da tamamilə repressiya edilmiş şəkildə kilidlədiyini düşünürdülər. Lakin MIT mühəndisləri müəyyən ediblər ki, hüceyrənin yaddaşı yalnız yandırma/söndürmə ilə deyil, həm də gen ifadəsinin daha pilləli, sönük kimi siferblat vasitəsilə qurulur. Kredit: İllüstrasiya Christine Daniloff, MIT; NIH Agentliyi
Hüceyrələr sağlam olduqda, onların hüceyrə tiplərini birdən dəyişməsini gözləmirik. Əlinizdəki dəri hüceyrəsi təbii olaraq beyin hüceyrəsinə çevrilməyəcək və əksinə. Bu, hüceyrənin həyatı boyu müxtəlif genlərin ifadəsini “bağlamağa” imkan verən epigenetik yaddaş sayəsindədir. Bu yaddaşın pozulması xərçəng kimi xəstəliklərə səbəb ola bilər.
Ənənəvi olaraq, elm adamları epigenetik yaddaşın daimi Lite-Brite nümunəsi kimi ya tam aktivləşdirilmiş, ya da tam repressiya edilmiş genləri ya “açıq” və ya “söndürülmüş” vəziyyətdə kilidlədiyini düşünürdülər . Lakin MIT mühəndisləri şəklin daha çox çalarları olduğunu tapdılar.
Bu gün Cell Genomics -də nəşr olunan yeni bir araşdırmada komanda, hüceyrənin yaddaşının yandırma/söndürmə ilə deyil, gen ifadəsinin daha pilləli, sönük kimi siferblat vasitəsilə qurulduğunu bildirir.
Tədqiqatçılar müxtəlif hüceyrələrdə fərqli səviyyələrdə tək bir genin ifadəsini təyin etdikləri təcrübələr həyata keçirdilər. Ənənəvi müdriklik genin nəhayət işə salınması və ya söndürülməsi lazım olduğunu güman etsə də, tədqiqatçılar genin orijinal ifadəsinin davam etdiyini tapdılar: Gen ifadəsi açıq və söndürülmə arasında bir spektr boyunca qurulmuş hüceyrələr bu aralıq vəziyyətdə qaldılar.
Nəticələr göstərir ki, epigenetik yaddaş – hüceyrələrin gen ifadəsini saxlaması və öz şəxsiyyətini “yadda saxlaması” prosesi – ikili deyil, əksinə, analoqdur, bu da gen ifadəsinin spektrinə və əlaqəli hüceyrə şəxsiyyətlərinə imkan verir.
MIT-də mexaniki və bioloji mühəndislik professoru, tədqiqat müəllifi Domitilla Del Vecchio deyir: “Bizim tapıntımız hüceyrələrin genləri yalnız açıq və ya söndürülməsi əvəzinə, gen ifadəsinin xüsusi səviyyələrində kilidləyərək, son şəxsiyyətlərini öhdəsinə götürmək imkanını açır”. “Nəticə, bədənimizdə bu gün bildiyimizdən və tanıdığımızdan daha çox hüceyrə növü ola bilər ki, bu da mühüm funksiyaları ola bilər və sağlam və ya xəstə vəziyyətlərin əsasını təşkil edə bilər.”
Tədqiqatın MIT-nin aparıcı müəllifləri Sebastian Palacios və Simone Bruno, əlavə həmmüəlliflərdir.
Binardan kənar
Hər hüceyrə eyni genomu paylaşır və bu, həyatın başlanğıc komponenti kimi düşünülə bilər. Hüceyrə forma aldıqda, genomunda olan genlərin ifadəsi ilə bu və ya digər tipə diferensiasiya olunur. Bəzi genlər aktivləşir, bəziləri isə repressiyaya məruz qalır. Kombinasiya hüceyrəni bir şəxsiyyətə qarşı digərinə yönləndirir.
Müəyyən molekulların genlərin DNT-sinə bağlandığı DNT metilasiyası prosesi onların ifadəsini yerində saxlamağa kömək edir. DNT metilasiyası hüceyrəyə gen ifadəsinin unikal modelini “yadda saxlamağa” kömək edir və nəticədə hüceyrənin şəxsiyyətini təyin edir.
Del Vecchio-nun MIT-dəki qrupu hüceyrə molekulyar prosesləri başa düşmək və yeni imkanlara malik hüceyrələrin mühəndisliyi üçün riyaziyyat və genetik mühəndisliyi tətbiq edir. Əvvəlki işində onun qrupu DNT metilasiyası və yumurtalıq hüceyrələrində müəyyən genlərin ifadəsini bloklamaq yolları ilə təcrübə edirdi.
Del Vecchio deyir: “Dərslik anlayışı, DNT metilasyonunun genləri ya açıq, ya da qapalı vəziyyətdə kilidləmək rolu idi” dedi. “Biz bunun dogma olduğunu düşündük. Lakin sonra buna uyğun olmayan nəticələr görməyə başladıq.”
Təcrübələrindəki hüceyrələrin bir çoxu genlərin hamısı və ya heç nə ifadəsini nümayiş etdirsə də, əhəmiyyətli sayda hüceyrənin genləri nə tamamilə açıq, nə də sönük vəziyyətdə dondurduğu ortaya çıxdı.
Palacios deyir: “Biz aşkar etdik ki, on və off arasında istənilən səviyyəni ifadə edən bir hüceyrə spektri var”. “Və düşündük ki, bu necə mümkündür?”
Gündəlik anlayışlar üçün Phys.org-a etibar edən 100.000-dən çox abunəçi ilə elm, texnologiya və kosmosda ən son yenilikləri kəşf edin . Pulsuz xəbər bülleteni üçün qeydiyyatdan keçin və mühüm nailiyyətlər, yeniliklər və tədqiqatlar haqqında gündəlik və ya həftəlik yeniləmələr əldə edin .
Mavi çalarları
Yeni araşdırmada komanda, müşahidə etdikləri aralardakı gen ifadəsinin təsadüfi, yoxsa bu günə qədər diqqətdən kənarda qalan hüceyrələrin daha çox yerləşmiş bir xüsusiyyəti olub-olmadığını öyrənmək məqsədi güdürdü.
Del Vecchio deyir: “Ola bilər ki, elm adamları aydın öhdəliyi olmayan hüceyrələrə məhəl qoymayıblar, çünki onlar bunun keçici bir vəziyyət olduğunu güman edirdilər”. “Amma əslində bu hüceyrələr arasında olan bu tiplər mühüm funksiyalara malik ola biləcək daimi vəziyyətlər ola bilər.”
Tədqiqatçılar fikirlərini yoxlamaq üçün hamster yumurtalıq hüceyrələri ilə təcrübələr apardılar – laboratoriyada çox istifadə olunan hüceyrələr xətti. Hər bir hüceyrədə bir mühəndislik gen əvvəlcə fərqli bir ifadə səviyyəsinə təyin edildi. Gen bəzi hüceyrələrdə tam işə salındı, digərlərində tamamilə söndürüldü və qalan hüceyrələr üçün açıq və söndürüldü.
Komanda mühəndis geni, genin ifadə səviyyəsinə uyğun parlaqlıqla yanan flüoresan markerlə qoşalaşdırdı. Tədqiqatçılar qısa müddət ərzində genin DNT metilasiyasını tetikleyen fermenti, təbii gen kilidləmə mexanizmini təqdim etdilər. Daha sonra onlar modifikasiyanın genləri öz aralarındakı ifadə səviyyələrində bağlayacağını və ya kilidlənmədən əvvəl genlərin tam açıq və ya qeyri-aktiv vəziyyətə miqrasiya edib-etməyəcəyini görmək üçün beş ay ərzində hüceyrələri izlədilər.
Del Vecchio deyir: “Bizim flüoresan markerimiz mavidir və biz hüceyrələrin bütün spektrdə parıldadığını görürük, həqiqətən parlaq mavidən tutmuş, tutqun və tutqun, ümumiyyətlə mavi olmayana qədər”. “Hər bir intensivlik səviyyəsi zamanla qorunur, bu o deməkdir ki, gen ifadəsi dərəcələndirilir və ya analoqdur, ikili deyil. Biz çox təəccübləndik, çünki bu qədər uzun müddətdən sonra genin sönəcəyini, ya tam açıq, ya da sönəcəyini düşündük, amma olmadı.”
Tapıntılar hüceyrənin genomunda müəyyən genlərin ifadəsini tənzimləməklə daha mürəkkəb süni toxumaların və orqanların mühəndisliyi üçün yeni yollar açır, məsələn, keçid deyil, radiodakı siferblat. Nəticələr həmçinin hüceyrənin epigenetik yaddaşının şəxsiyyətini müəyyən etmək üçün necə işlədiyinə dair mənzərəni çətinləşdirir. Terapiyaya davamlı şişlərdə nümayiş etdirilən hüceyrə modifikasiyalarının daha dəqiq şəkildə müalicə oluna bilməsi ehtimalını açır.
Kaliforniya Texnologiya İnstitutunun biologiya və bioloji mühəndislik professoru , tədqiqatda iştirak etməyən Michael Elowitz deyir: “Del Vecchio və həmkarları analoq yaddaşın DNT-nin özündə kimyəvi modifikasiyalar vasitəsilə necə yarandığını gözəl şəkildə göstərdilər”. “Nəticədə, biz indi təkamül yolu ilə icad edilmiş bu təbii analoq yaddaş mexanizminin sintetik biologiya sahəsində dəyişdirilməsini təsəvvür edə bilərik ki, bu da bizə daimi və dəqiq çoxhüceyrəli davranışları proqramlaşdırmağa kömək edə bilər.”
Palacios deyir: “İnsanlarda mürəkkəbliyi təmin edən şeylərdən biri epigenetik yaddaşdır”. “Və biz bunun düşündüyümüz kimi olmadığını görürük. Mənim üçün bu, əslində ağıllara sovrulur. Və düşünürəm ki, biz bu analoq yaddaşın biologiyada bir çox müxtəlif proseslər üçün aktual olduğunu görəcəyik.”
Daha çox məlumat: Sebastian Palacios et al, Məqsədli xromatin redaktəsi ilə aşkar edilən analoq epigenetik yaddaş, Cell Genomics (2025). DOI: 10.1016/j.xgen.2025.100985 . bioRxiv DOI- də : 10.1101/2024.02.13.580200
Jurnal məlumatı: bioRxiv , Cell Genomics
Massaçusets Texnologiya İnstitutu tərəfindən təmin edilmişdir