In situ genom sıralama innovasiyasının genişlənməsi gizli DNT-zülal qarşılıqlı təsirlərini görünən edir
Harvard alimləri mövcud in situ genom sıralamasını (IGS) genişlənmə mikroskopiyası (ExM) ilə birləşdirən genişlənmə in situ genom ardıcıllığı (ExIGS) adlı yeni texnikanı təqdim ediblər. Yenilik tədqiqatçılara nüvə anomaliyalarını nanometr miqyasda DNT-zülal qarşılıqlı təsirlərinin dəqiq ölçülməsi ilə bir hüceyrə daxilində gen tənzimlənməsindəki dəyişikliklərlə əlaqələndirməyə imkan verdi.
Mikroskopiya hüceyrə funksiyasını xarakterizə etmək üçün vacib bir vasitədir. Təsvir üsulları optik mikroskopiyanın difraksiya həddi ilə məhdudlaşır, DNT-zülal qarşılıqlı təsirləri miqyasında etibarlı ölçmənin qarşısını alır.
Genişlənmə mikroskopiyası, difraksiya həddinin gizlətdiyi şeyləri böyüdərək görmə problemini aradan qaldıran ağıllı bir texnikadır . Nümunəni şişən bir polimer gelə yerləşdirməklə və genişləndirməklə, tədqiqatçılar adi mikroskoplardan istifadə edərək hüceyrələr daxilində məkan təşkilatlarının yüksək keyfiyyətli təsvirini əldə edə bilərlər.
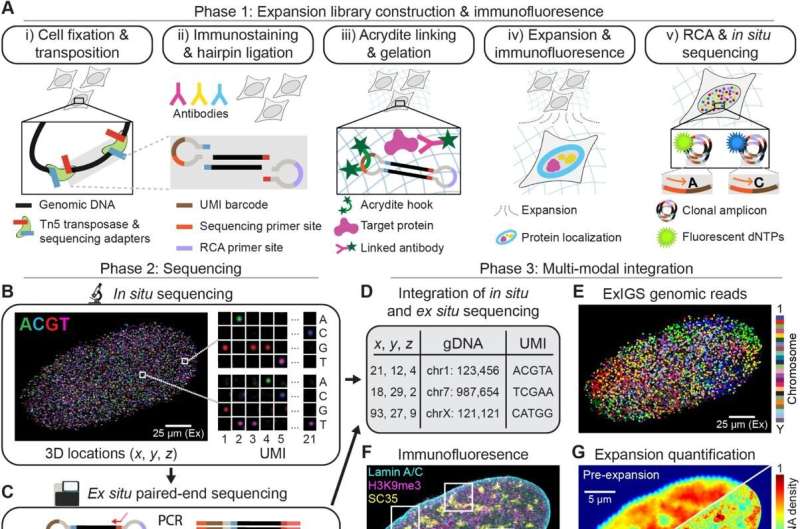
ExIGS-də genomik DNT-ni və nüvə zülallarını tək hüceyrələr daxilində nanoölçülü rezolyusiyada eyni vaxtda ardıcıllaşdırmaq üçün genişlənmə mikroskopiyası in situ genom ardıcıllığı ilə inteqrasiya olunur.
Proses, genişlənmə üçün iskele kimi xidmət edən poliakrilat əsaslı bir gelə sabit hüceyrələrin yerləşdirilməsi ilə başlayır. Genomik DNT və zülallar, genomik fraqmentlərə və zülallara birləşdirilmiş DNT saç sancaqlarına bağlanan DNT oliqo qarmaqlarından istifadə edərək gellə kimyəvi cəhətdən əlaqələndirilir. Bu qarmaqlar polimerləşmə zamanı gel ilə kovalent bağlar yaradan kimyəvi qrupları ehtiva edir.Oyna
00:0000:03SəssizParametrlərPIPTam ekrana daxil olun
Yerləşdirildikdən sonra gel sabit hüceyrə komponentləri ətrafında polimerləşərək DNT və zülalları hərəkətsizləşdirir. Su gelə əlavə edilir və onun bütün istiqamətlərdə təxminən 4,5-5,5 dəfə bərabər şişməsinə səbəb olur. Bu genişlənmə molekullar arasındakı məkan əlaqəsini qoruyaraq hüceyrəni fiziki olaraq genişləndirir. Yeni genişlənmiş strukturun bütövlüyünü qorumaq üçün nümunə daha sonra ikincil genişlənməyən akrilamid gelə yenidən daxil edilir.
https://googleads.g.doubleclick.net/pagead/ads?gdpr=0&us_privacy=1—&gpp_sid=-1&client=ca-pub-0536483524803400&output=html&h=188&slotname=8188791252&adk=1687169288&adf=1857921027&pi=t.ma~as.8188791252&w=750&abgtt=6&fwrn=4&lmt=1728973646&rafmt=11&format=750×188&url=https%3A%2F%2Fphys.org%2Fnews%2F2024-10-expansion-situ-genome-sequencing-hidden.html&wgl=1&uach=WyJXaW5kb3dzIiwiMTUuMC4wIiwieDg2IiwiIiwiMTI5LjAuNjY2OC45MCIsbnVsbCwwLG51bGwsIjY0IixbWyJHb29nbGUgQ2hyb21lIiwiMTI5LjAuNjY2OC45MCJdLFsiTm90PUE_QnJhbmQiLCI4LjAuMC4wIl0sWyJDaHJvbWl1bSIsIjEyOS4wLjY2NjguOTAiXV0sMF0.&dt=1728971752779&bpp=1&bdt=85&idt=73&shv=r20241010&mjsv=m202410080101&ptt=9&saldr=aa&abxe=1&cookie=ID%3Ddd084782a3980897%3AT%3D1725971170%3ART%3D1728973430%3AS%3DALNI_Ma1uv12HX_ctV-7loP2Dla_dLGslw&eo_id_str=ID%3D6cdee71e935b6dcb%3AT%3D1725971170%3ART%3D1728973430%3AS%3DAA-AfjZEH1DAbfRV50frmhACTroQ&prev_fmts=0x0&nras=1&correlator=5533426171221&frm=20&pv=1&rplot=4&u_tz=240&u_his=1&u_h=1080&u_w=1920&u_ah=1032&u_aw=1920&u_cd=24&u_sd=1&dmc=8&adx=447&ady=2866&biw=1903&bih=911&scr_x=0&scr_y=0&eid=44759876%2C44759927%2C44759837%2C31087701%2C31087805%2C31087891%2C95343455%2C95344190%2C95344778&oid=2&pvsid=2861338981820780&tmod=365233425&uas=0&nvt=1&ref=https%3A%2F%2Fphys.org%2Fsort%2Fdate%2Fall%2Fpage8.html&fc=1920&brdim=0%2C0%2C0%2C0%2C1920%2C0%2C0%2C0%2C1920%2C911&vis=1&rsz=%7C%7CpeEbr%7C&abl=CS&pfx=0&fu=128&bc=31&bz=0&td=1&tdf=2&psd=W251bGwsbnVsbCxudWxsLDNd&nt=1&ifi=2&uci=a!2&btvi=1&fsb=1&dtd=M
Genişləndirilmiş nümunə nüvə zülallarının təfərrüatlı vizuallaşdırılmasına imkan verən yüksək rezolyusiyaya malik immunofluoresan görüntüləmədən keçir. Daha sonra in situ ardıcıllıqla klonal DNT amplikonları yaratmaq üçün yuvarlanan dairənin gücləndirilməsi həyata keçirilir. Bu gücləndirmə genişlənmiş nüvə daxilində genomik DNT-nin dəqiq ardıcıllığını və lokalizasiyasını təmin edir.
Tədqiqatçılar bioRxiv preprint serverində “İn situ genom ardıcıllığının genişləndirilməsi nüvə anormallıqlarını aberrant euxromatin repressiyasının qaynar nöqtələri ilə əlaqələndirir” adlı çapdan əvvəl hazırladıqları məqalədə öz innovasiyalarının sınaqdan keçirilməsini təfərrüatlı şəkildə izah edirlər .
Tədqiqatçılar Hutchinson-Gilford progeria sindromu olan bir xəstənin fibroblast hüceyrələrinə ExIGS tətbiq etməklə, nüvə laminlərində (nüvəyə struktur verən zülallar) pozğunluqları müəyyən etdilər ki, bu da aktiv genomik bölgələrdə anormal repressiya nöqtələri yaradan, potensial olaraq hüceyrə şəxsiyyətini pozur.
Tədqiqat göstərdi ki, ExIGS nüvəyə düşən genomik oxunmaların sayını əhəmiyyətli dərəcədə artırır və Hi-C sıralama məlumatları ilə müqayisə edilə bilən 3D genom strukturunu qoruyur.
Texnika DNT-zülal qarşılıqlı əlaqəsini araşdırmaq üçün yeni güclü platforma təqdim edir və tədqiqatçılara molekulyar mexanizmlərin görünməmiş görünüşünə imkan verir. O, geniş spektrli xəstəliklər və genetik pozğunluqlar haqqında anlayışımızı əhəmiyyətli dərəcədə artıra, qocalma zamanı hüceyrə qocalmasının gizli qarşılıqlı təsirlərini aşkar edə və biotexnologiya tədqiqat laboratoriyalarında pozucu texnologiyaya çevrilə bilər.
Daha çox məlumat: Ajay S. Labade et al, Expansionin situgenome ardıcıllığı nüvə anormallıqlarını aberrant euchromatin repressiyasının qaynar nöqtələri ilə əlaqələndirir, bioRxiv (2024). DOI: 10.1101/2024.09.24.614614
Jurnal məlumatı: bioRxiv