Keçmiş donanma mexaniki irsi Alzheimer xəstəliyinin genetik ehtimallarına necə qarşı çıxdı
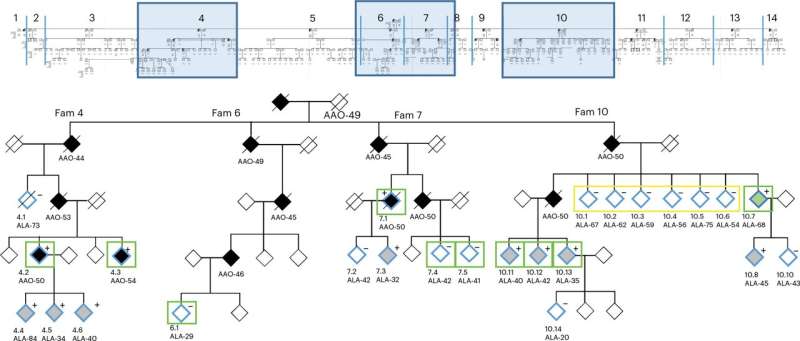
Sent-Luisdəki Vaşinqton Universiteti Tibb Məktəbinin tədqiqatçıları presenilin 2 (PSEN2) p.Asn141Ile mutasiyasını, dominant irsi Alzheimer xəstəliyinə (DIAD) səbəb olduğu bilinən genetik variantı daşıyan fərd üzərində uzununa araşdırma aparıblar. Yüksək riskli fərd, gözlənilən klinik başlanğıc yaşından 18 il keçməsinə baxmayaraq, koqnitiv olaraq bütöv qalmışdır. Tədqiqatçılar potensial qoruyucu mexanizmləri anlamaq üçün genetik, neyroimaging və biomarker məlumatlarını araşdırdılar.
Tipik DIAD inkişafından fərqli olaraq, bu vəziyyətdə tau patologiyası yayılmadan oksipital lobla məhdudlaşır və idrakın azalmasının olmaması üçün mümkün izahat verir.
DIAD amiloid prekursor zülalında (APP), presenilin 1 (PSEN1) və ya PSEN2-də anormal amiloid-β emalına və erkən başlanğıc Alzheimer xəstəliyinə səbəb olan yüksək nüfuz edən mutasiyaların nəticəsidir . Dominant İrsi Alzheimer Şəbəkəsi (DIAN) DIAD mutasiya daşıyıcılarını izləmək və zamanla klinik, koqnitiv və biomarker dəyişikliklərini qiymətləndirmək üçün yaradılmışdır.
Əvvəlki tədqiqatlar mutasiya daşıyıcılarında AD-yə müqavimət göstərə bilən nadir genetik variantlar müəyyən etmişdi , lakin belə hallar olduqca nadir olaraq qalır.
Təbiət Təbabətində nəşr olunan “Demensiyadan qorunan dominant irsi Alzheimer xəstəliyi mutasiya daşıyıcısının uzunlamasına analizi” adlı araşdırmada tədqiqatçılar on il ərzində iştirakçının genetik profilini, koqnitiv funksiyasını, neyroimaging məlumatlarını və biomarker səviyyələrini araşdırdılar.
PSEN2 p.Asn141Ile mutasiyasını daşıyan böyük ailənin üzvü olan iştirakçı, gözlənilən xəstəliyin başlanğıc yaşından çox asimptomatik olaraq qaldı. Ailə tarixinin təhlili göstərdi ki, iştirakçının 13 ana xalası və dayısından 11-i 50 yaşa qədər AD inkişaf etdirdi. Ailəyə məxsus məlumatlara əsasən, bu mutasiya üçün orta simptomatik yaş 53,7 ildir, lakin bu fərd 71 yaşında koqnitiv olaraq normal olaraq qalır.
2011-ci ildə DIAN tədqiqatına yazıldıqdan sonra klinik və koqnitiv qiymətləndirmələr ardıcıl olaraq heç bir dəyər itirmə əlaməti göstərmir. İştirakçı 2011 və 2021-ci illər arasında çoxsaylı qiymətləndirmələrdə Klinik Demans Reytinqini 0 və Mini-Psixi Dövlət İmtahan balı 30 olaraq saxladı. Nöropsikiyatrik və funksional qiymətləndirmələr əhəmiyyətli bir azalma göstərmədi, baxmayaraq ki, bəzi koqnitiv test xalları emal sürəti və icra funksiyasında cüzi azalmalar göstərdi. Nevroloji müayinələr ilk dəfə 2017-ci ildə qeyd edilən sağ əldə yalnız yüngül postural tremor aşkar etdi.
Neyroimaging oksipital lobda lokallaşdırılmış tau çöküntüsünün atipik nümunəsini aşkar etdi, bu tapıntı tipik DIAD irəliləməsi ilə uyğun gəlmir. Amiloid-β çökməsi simptomatik DIAD mutasiya daşıyıcıları ilə müqayisə oluna bilsə də, tau yığılması oksipital korteksdən kənara yayılmadı və bu, potensial olaraq bilişsel geriləmənin olmamasını izah etdi.
Maqnit rezonans görüntüləmə hipokampal həcmdə tədricən, yaşa uyğun azalma göstərdi, pozitron emissiya tomoqrafiyası (PET) isə simptomatik DIAD daşıyıcıları ilə müqayisədə qlükoza qəbulunda məhdud metabolik dəyişiklikləri təsdiqlədi.
Bütün genom ardıcıllığı APOE3-Christchurch (p.Arg136Ser) və ya RELN p.His3447Arg kimi digər autosomal dominant Alzheimer Xəstəliyi hallarında davamlılıqla əlaqəli olan əvvəllər məlum olan qoruyucu variantları müəyyən etməmişdir.
Bununla belə, genetik analiz FAM151B, CHST15, CEP290, GPCPD1 və PRICKLE3 kimi genlərdə AD-yə qarşı müqavimətdə rol oynaya bilən nadir kodlaşdırma variantlarını müəyyən etdi. İştirakçı həmçinin AD riski ilə qeyri-müəyyən əlaqəsi olan TREM2 p.Asp87Asn variantını və tau patologiyasına təsir göstərə bilən MAPT variantını (p.Tyr441His) daşıyırdı.
Ətraf mühit amilləri
İştirakçı, tez-tez soyutma tədbirləri tələb edən dəniz dizel mexaniki olaraq yüksək istiyə uzun müddət məruz qalmışdır. Proteomik analiz zülalların qatlanmasında və neyroproteksiyada rol oynaya bilən istilik şoku zülallarının yüksək səviyyələrini aşkar etdi. Erkən yaşda bu təcrübə və bədənin buna reaksiyası ömür boyu dayanıqlılığa töhfə vermiş ola bilər.
Uzunlamasına serebrospinal maye və plazma biomarker analizləri amiloid-β səviyyələrinin və amiloid-β42/40 nisbətlərinin simptomatik DIAD daşıyıcılarında müşahidə edilən diapazonda olduğunu göstərdi. Fosforilləşdirilmiş tau markerləri (pTau181, pTau217, pTau205) DIAD daşıyıcıları və daşıyıcı olmayanlar arasında aralıq idi və bu, tau patologiyasında potensial dəyişiklikləri təklif edir.
Proteomik və metabolomik analizlər neyrodejenerasiyaya qarşı müqavimətə kömək edə biləcək protein sintezi, metabolizm və anti-oksidləşdirici stress reaksiyaları ilə bağlı yollarda dəyişiklikləri müəyyən etdi.
Bu, gözlənilən klinik kursa zidd olan DIAD mutasiya daşıyıcısının nadir nümunəsidir və AD inkişafında genetik, bioloji və ətraf mühit amilləri arasında qarşılıqlı əlaqə haqqında yeni suallar doğurur. Müqavimətin dəqiq mexanizmləri bəlli olmasa da, məhdud tau patologiyası həlledici rol oynaya bilər. Tau yayılmasının qarşısının alınmasının Alzheimer xəstəliyinin gecikdirilməsi və ya qarşısının alınması üçün terapevtik strategiya kimi xidmət edə biləcəyini müəyyən etmək üçün əlavə tədqiqatlara ehtiyac var.
Daha çox məlumat: Jorge J. Llibre-Guerra et al, Demansdan qorunan dominant irsi Alzheimer xəstəliyi mutasiya daşıyıcısının uzununa təhlili, Təbiət Medicine (2025). DOI: 10.1038/s41591-025-03494-0
Jurnal məlumatı: Nature Medicine
© 2025 Science X Network