Mayeyəbənzər histon H1 nukleosomları “yapışdırır” və DNT-nin necə sıxlaşdığını dəyişdirir
İnformasiya və Sistemlər üzrə Tədqiqat Təşkilatı tərəfindən
Sadie Harley tərəfindən redaktə edilib , Robert Egan tərəfindən nəzərdən keçirilib
Tercih edilən mənbə kimi əlavə edin
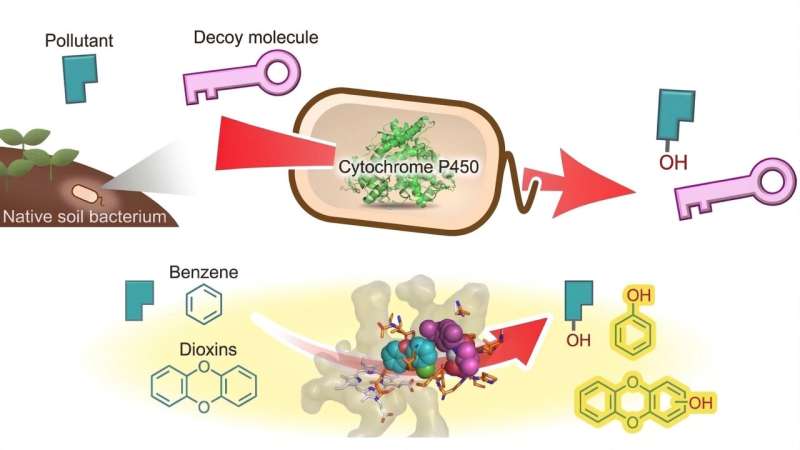
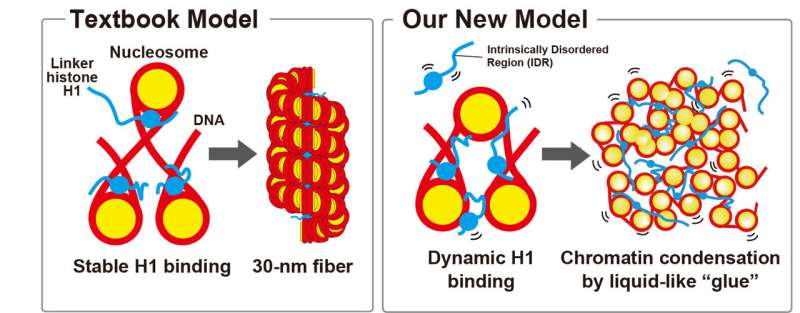
Əvvəllər, bağlayıcı histon H1-in nizamlı, “sərt” bir quruluş yaratmaqla nukleosomlara və kompakt xromatinə sabit şəkildə bağlandığı düşünülürdü (solda). Bu tədqiqatda biz göstəririk ki, H1 dinamik olaraq nukleosomlara bağlanır və mayeyə bənzər “yapışqan” kimi hərəkət edərək xromatini sıxlaşdırır, eyni zamanda dinamik, mayeyə bənzər bir təşkilat yaradır (sağda). Müəllif: Masa A. Şimazoe, Saçiko Tamura və Kazuhiro Maeşima, Milli Genetika İnstitutu, ROIS
Nüvənin içərisindəki DNT sərt nizamlı lif kimi yığılmayıb — H1 histonu dinamik olaraq nukleosomları bir-birinə bağlayır və boş şəkildə “yapışdırır”, bununla da hələ də vacib genom funksiyalarını dəstəkləyə bilən dinamik, maye bir təşkilat yaradır.
İnsan genomu sıxlaşmaq üçün əlamətdar bir qabiliyyətə malikdir. Əgər bütün 46 insan xromosomu başdan-ayağa uzansaydı, ümumi uzunluğu təxminən iki metrə çatardı, lakin onlar nədənsə diametri cəmi 10 mikrometr olan bir nüvədə yerləşirlər.
Nüvənin içinə sığmaq üçün DNT, makara ətrafındakı ip kimi histon zülallarına sarılır və nukleosomlar əmələ gətirir. Nükleosomlar və əlaqəli zülallar daha sonra xromatinə qatlanır və bu da genomun funksional olaraq qalaraq qablaşdırılmasına imkan verir.
H1-in xromatini necə sıxlaşdırdığını yenidən düşünmək
Onilliklər ərzində molekulyar biologiya dərsliklərində bağlayıcı histon H1 nukleosomları müntəzəm, sərt yüksək tərtibli strukturlara (çox vaxt 30 nm xromatin lifi kimi təsvir olunur) təşkil edən əsas amil kimi təsvir edilmişdir. Lakin toplanmış dəlillər göstərir ki, bu cür yüksək tərtibli liflər canlı hüceyrələrdə çox nadirdir. Bu, fundamental bir sual doğurur: H1 əslində DNT-ni necə sıxlaşdırır və xromatini in vivo təşkil edir?Oyna
00:00
00:30SəssizParametrlərPIPTam ekrana daxil olun
Yaponiyadakı SOKENDAI və Milli Genetika İnstitutunun (İnformasiya Sistemləri Tədqiqat Təşkilatı, ROIS) professoru Kazuhiro Maeşimanın və Böyük Britaniyadakı Kembric Universitetinin professoru Rosana Collepardo-Gevaranın rəhbərlik etdiyi bir qrup, H1-in canlı insan hüceyrələrinin içərisində nukleosomlara necə bağlandığını və xromatini necə formalaşdırdığını araşdırdı.
Tədqiqatçılar tək nukleosom görüntüləməsini super qətnaməli flüoresans mikroskopiyası və hesablama modelləşdirməsi ilə birləşdirərək H1 funksiyasının yeni bir fiziki mənzərəsini ortaya qoyurlar: H1 statik sıxac kimi işləmək əvəzinə, xromatini digər molekullar üçün əlçatan qalan maye quruluşuna yumşaq bir şəkildə qatlayan dinamik, mayeyə bənzər bir “yapışqan” kimi davranır.
Komanda nəticələrini Science Advances jurnalında dərc edib .
Maeşima bildirib ki, “Nəticələrimiz göstərir ki, H1 sadəcə xromatini sərt lifə bağlayan “statik sıxac” deyil. Bunun əvəzinə, H1 dinamik olaraq nukleosomlarla əlaqə qurur və daha çox maye kimi yapışqan kimi hərəkət edir – dinamik, uyğunlaşa bilən bir təşkilatı qoruyarkən xromatinin kondensasiyasına kömək edir.”
Xromatinin canlı hüceyrələrin içərisində hərəkətini izləmək
Canlı hüceyrələrdə fərdi nukleosomların miqyasında xromatini müşahidə etmək üçün komanda, nukleosomları seyrək şəkildə flüoresansla etiketləyən və super qətnaməli lokalizasiya və hərəkət izləməsini təmin edən bir strategiyadan istifadə etdi. Təcrübələr göstərdi ki, H1 vasitəçiliyi ilə xromatin kondensasiyası yüksək nizamlı, sərt liflər əmələ gətirmədən əldə edilə bilər.
Masa A. Şimazoe bildirib ki, “Yüksək fəza qətnaməsində canlı hüceyrələrdəki nukleosomları izləməklə, xromatinin sərt bir quruluş kimi, yoxsa daha dinamik bir şey kimi davrandığını birbaşa sınaqdan keçirə bilərik. Gördüyümüz şey, H1-in yüksək dinamik şəkildə bağlanması və açılması ilə uyğun olan sıx, lakin maye bir təşkilatdır.”
Simulyasiyalar H1-in maye kimi yapışqan rolunu ortaya qoyur
Görüntüləmə müşahidələrini əsas fiziki mexanizmlə əlaqələndirmək üçün tədqiqatçılar xromatinin iri dənəli modellərini hazırladılar. Atomlara yaxın molekulyar dinamika (MD) simulyasiyalarından istifadə edərək, onlar H1-xromatin qarşılıqlı təsirlərinin sıxılmaya, təşkilatlanmaya və dinamikaya necə təsir edəcəyini qiymətləndirdilər.
Rosana Collepardo-Gevara və Jan Huertas bildiriblər ki, “Simulyasiyalarımız bizə yaxınlaşmağa və H1-in xromatini necə formalaşdırdığı mikroskopik qaydaları aşkar etməyə imkan verir”.
“H1-in niyə dinamik, mayeyə bənzər yapışqan kimi çıxış etdiyini görəndə çox həyəcanlandıq: çoxlu nukleosomlar arasında çoxvalentli qarşılıqlı təsirlər yaratmaqla H1, xromatini sərt bir quruluşa bağlamadan bir yerdə saxlayan çevik bir şəbəkə qurur. Bu, H1-dəki kiçik dəyişikliklərin genomu daha böyük miqyasda necə yenidən formalaşdıra biləcəyini göstərir.”
Niyə maye genom hüceyrələr üçün vacibdir
Genom funksiyası transkripsiya, replikasiya və təmir üçün DNT-yə daxil olmaq üçün böyük protein birləşmələri tələb etdiyindən, tədqiqatçılar maye kimi xromatin təşkilatının üstünlük təşkil etdiyini irəli sürürlər: xromatin digər molekulyar maşınların nüfuz etməsinə və işləməsinə imkan verərkən kompakt qala bilər.
Maeşima bildirib ki, “Canlı hüceyrələrdə xromatinin fiziki təbiətini anlamaq, genomun necə oxunduğunu, kopyalandığını və saxlanıldığını izah etmək üçün vacibdir”.
“Bu iş H1 üçün yeni konseptual model təqdim edir və anormal H1 funksiyasının genom disrequlyasiyasına və xəstəliklərə necə təsir etdiyini anlamağımıza kömək edə bilər.”