Nanopartiküllər bir neçə insan hüceyrə növünü genetik olaraq dəyişdirə bilər
Derek Smit, Miçiqan Universiteti tərəfindən
Stephanie Baum tərəfindən redaktə edilib , Robert Egan tərəfindən nəzərdən keçirilib
Tercih edilən mənbə kimi əlavə edin
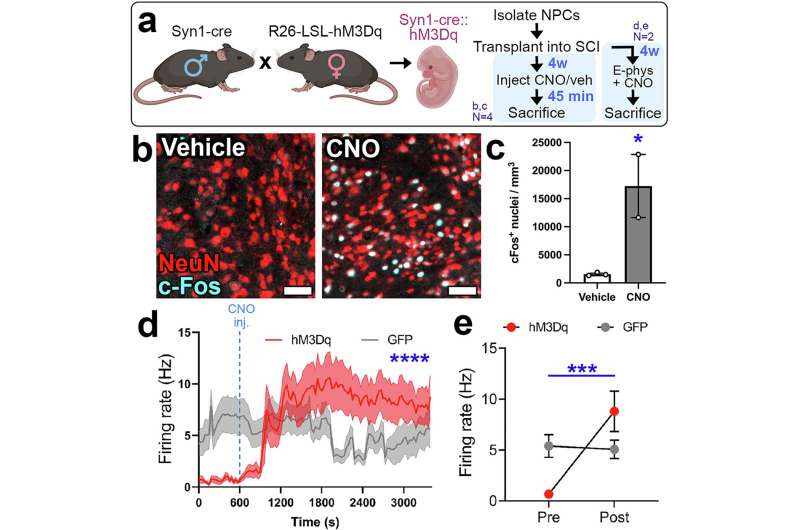
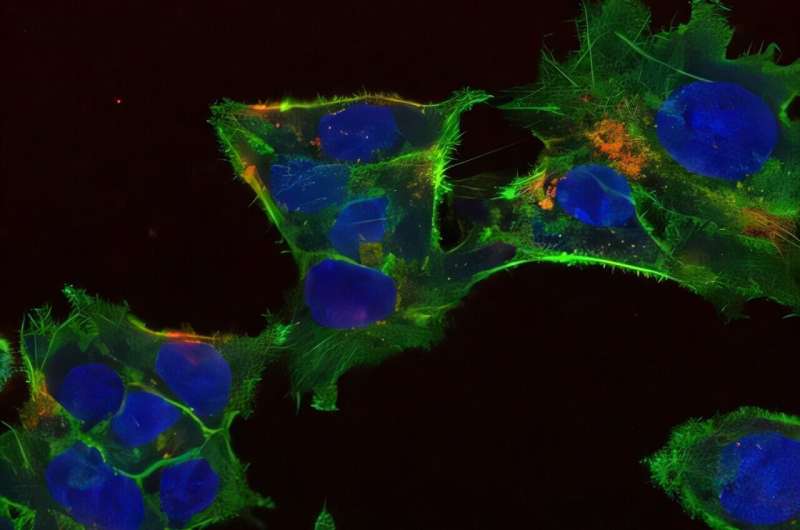
İnsan qaraciyər hüceyrələri hüceyrələri genetik olaraq dəyişdirən dairəvi (plazmid) DNT ilə yüklənmiş zülal nanopartikullarını udur. Konfokal lazer skanlama mikroskopiyası ilə çəkilmiş fotoda nanopartikullar qırmızı nöqtələrə bənzəyir və hüceyrələr yaşıl rəngdədir və DNT-nin saxlanıldığı və emal olunduğu mavi nüvəyə malikdir. Müəllif: Yao Yao, Lahann Laboratoriyası / Miçiqan Universiteti
Daha az yan təsirləri olan gen terapiyalarının yolunu açmağa kömək edə biləcək bir nümayişdə, Miçiqan Universiteti Mühəndislik və Miçiqan Tibbində hazırlanmış zülal nanopartikülləri ilə bir neçə insan hüceyrə növü genetik olaraq modifikasiya edilmişdir. Gen terapiyası oraq hüceyrəli anemiya və lösemi də daxil olmaqla qan xəstəliklərinin müalicəsində olduqca uğurlu olmuşdur. Lakin virusun müalicə üçün vektor kimi istifadəsi ikinci dərəcəli xərçəng və immun sisteminin həddindən artıq reaksiyaları kimi arzuolunmaz yan təsirlərə səbəb ola bilər. Nanopartiküllərlə tədqiqat qrupu gen terapiyalarının tətbiqi üçün daha təhlükəsiz bir metod hazırlamağı hədəfləyir.
Konsepsiyanın sübutu ilə aparılan təcrübədə tədqiqatçılar bir neçə növ insan hüceyrəsini modifikasiya etmək üçün nanopartikullardan istifadə ediblər. Onlar insan qaraciyər xərçəngi hüceyrələrinə, böyrək hüceyrələrinə və immun hüceyrələrinə yaşıl flüoresan zülal genləri verərək onları yaşıl rəngdə parıldatmağa məcbur ediblər. Hüceyrələr nanopartikulları udaraq həzm etdikdən sonra yeni genləri aktivləşdirərək içəridə olan DNT və ya xəbərçi RNT-ni buraxıblar. İş ” Advanced Materials” jurnalında dərc olunub .
“Tək bir mutasiya səbəbindən bir zülalın çatışmadığı və ya disfunksiyası olduğu bir çox xəstəlik var və biz yeni bir gen təqdim etməklə bunu mütləq düzəldə bilərik”, – deyə UM Biointerfaces İnstitutunun direktoru və tədqiqatın müvafiq müəllifi olan Volfqanq Pauli Kollecinin Kimya Mühəndisliyi professoru Joerg Lahann bildirib.
“Adətən, bu, viruslarla edilir, lakin viruslar zəhərli ola və immun hüceyrələrini aktivləşdirə bilər. Buna görə də, virus əsaslı gen redaktə strategiyalarının əvəz edilməsi üçün sahədə irəliləyişlər olub.”
Süni virus iflasa uğrayır
Gen redaktəsi artıq FDA tərəfindən təsdiqlənmiş qan və sümük iliyi xərçəngi, oraq hüceyrəli və beta-talassemiya müalicələrinin mərkəzi komponentidir. Bunlara immun hüceyrələrinin və ya qan kök hüceyrələrinin genetik modifikasiya olunmuş HİV variantı ilə toplanması və redaktə edilməsi daxildir ki, bu da immun hüceyrələrinin genomuna daxil olmaq üçün təkamül keçirib. Gen terapiyasında həkimlər virusu elə dəyişdirirlər ki, o, məsələn, qanın oksigen daşımasını yaxşılaşdıran və ya immun sisteminin xərçəng hüceyrələrini tanımasına və öldürməsinə kömək edən faydalı genlər təmin etsin. Redaktə edilmiş hüceyrələr daha sonra xəstəyə qaytarılır.
CAR T-hüceyrə terapiyası adlanan xərçəng terapiyası alan böyüklərin və uşaqların təxminən 80%-də xərçəngin tam remissiyası müşahidə olunur və gen terapiyaları oraq hüceyrəli xəstələrinin 88%-də və beta-talassemiya xəstələrinin 89%-də təsirli olur. Lakin bəzi xərçəng xəstələrində immun hüceyrələrinin ikinci xərçəngi, bəzi oraq hüceyrəli xəstələrdə isə qan xərçəngi inkişaf edir. Araşdırmalar göstərir ki, yeni xərçənglərə virus səbəb olur və bu virus şişi yatıran genləri öz içinə soxaraq parçalayır.
Qida və Dərman Administrasiyası (FDA) dəri xərçəngi , anadangəlmə korluq və onurğa əzələ atrofiyası ilə mübarizə aparmaq üçün bədənə birbaşa inyeksiya üçün digər virusları təsdiqləyib , lakin bu viruslar bəzən infeksiyalara və təhlükəli immun reaksiyalarına səbəb ola bilər .Kimya mühəndisliyi üzrə doktorantura tələbəsi Fjorela Xhyliu (sağda) və Volfqanq Pauli adına Kimya mühəndisliyi üzrə Kollec professoru Joerg Lahann (solda) elektrohidrodinamik axın prosesinin işlədiyini yoxlamaq üçün yaşıl lazerdən istifadə edirlər. Lazer, zülal və DNT qarışığı şprisin altındakı alüminium lövhəyə axıdıldıqda incə bir duman aşkar edir. Müəllif: Gabi Iriarte, Miçiqan Mühəndislik Universiteti
Tədqiqatçıların nanopartikulları gen terapiyası zamanı yeni xərçənglərin qarşısını almağa kömək edə bilər, çünki halqa formalı (plazmid) DNT və ya RNT xəstənin genomuna daxil edilmir, buna görə də heç bir gen parçalanmır. Zülalın xarici örtüyü həmçinin iltihaba, qızdırmaya və qaraciyərə zərər verə biləcək mövcud yağ əsaslı (lipid) nanopartikullardan daha təhlükəsiz ola bilər .
Tədqiqatçıların təcrübələrində seçim zülalı qanın təbii komponenti olan serum albumin idi . UM Tibb Məktəbinin klinik müəllimi, həmmüəllif Maykl Tribvasserin sözlərinə görə, gələcək reseptlərdə nanopartikulların müəyyən hüceyrə tiplərinə daxil olmasına kömək etmək üçün neyrotransmitterlər və ya siqnal zülalları kimi digər zülallardan istifadə edilə bilər.
Gündəlik məlumat üçün Phys.org-a etibar edən 100.000-dən çox abunəçi ilə elm, texnologiya və kosmosdakı ən son yenilikləri kəşf edin . Pulsuz bülletenimizə abunə olun və vacib olan nailiyyətlər, innovasiyalar və tədqiqatlar haqqında gündəlik və ya həftəlik yeniliklərdən xəbərdar olun .
Genlər necə çatdırılır
Nanohissəciklər elektrohidrodinamik (EHD) axın adlanan çap texnikası ilə hazırlanır. Əvvəlcə zülal suda ya DNT, ya da RNT ilə qarışdırılır və alüminium lövhənin üzərində asılmış şprisə yerləşdirilir. Daha sonra tədqiqatçılar yüklü zülalı, genetik materialı və suyu şprisdən yüksək sürətlə çıxaran elektrik sahəsi tətbiq edirlər. Sürətlənmə suyu tez bir zamanda buxarlandırır və zülalı genetik materialın ətrafında kondensasiya edir. Daha sonra tədqiqatçılar hissəcikləri bir yerdə saxlamaq üçün polietilenimin adlı sintetik, geləbənzər kimyəvi maddəyə sarırlar.
Hüceyrələr hissəcikləri udduqdan sonra, hüceyrələrin qidanı həzm etdiyi və ya patogenləri öldürdüyü endosom adlanan qabarcıq şəkilli bölmələrdə ilişib qalırlar. Nanohissəciklər həzm olunduqca, müsbət yüklü polietilenimin yük balanssızlığı yaradır. Su endosoma daxil olur, onu partladır və genetik materialı buraxır.
Sərbəst buraxılan genetik material hüceyrənin DNT-sinə inteqrasiya edilmədən təsirlər daimi olmayacaq – mRNT bir neçə gün, plazmid DNT isə maksimum bir neçə ay davam edir. Həll yolu olaraq, xəstələr “gücləndirici” dozalar ala bilərlər. Nanopartiküllər, genləri xəstənin genomuna viruslardan daha dəqiq daxil edən bir protein olan CRISPR-Cas9 ilə yükləndikdə “birdəfəlik” müalicəyə çevrilə bilər.
“Gələcək tədqiqatlarda nanopartikulların insan hüceyrələrini terapevtik genlərlə dəyişdirmək və potensial yan təsirləri müəyyən etmək qabiliyyətini sınaqdan keçirməyə ümid edirik”, – deyə kimya mühəndisliyi üzrə doktorantura məzunu və UM Stomatologiya Məktəbinin səhiyyə elmləri üzrə doktorantura məzunu Yao Yao və UM-nin kimya mühəndisliyi üzrə keçmiş doktoranturadan sonrakı tədqiqatçısı Yeongun Ko ilə birlikdə tədqiqatın həmmüəllifi olan Fjorela Xhyliu bildirib.