Potensial xərçəng əleyhinə agentin sınaqları niyə dayandırılıb: Yeni ferment anlayışları məhsuldarlığı və təmizliyi artıra bilər
Theresa Hübner, Bayreuth Universiteti tərəfindən
Lisa Lock tərəfindən redaktə edilib , Robert Egan tərəfindən nəzərdən keçirilib
Tercih edilən mənbə kimi əlavə edin
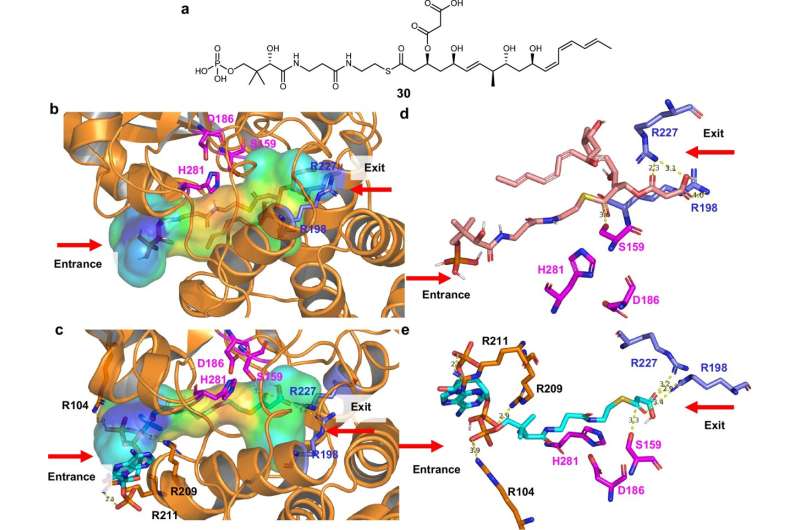
Qeyri-kanonik β-O-malonilləşmə üçün struktur əsas. Müəllif: Nature Communications (2026). DOI: 10.1038/s41467-026-70144-5
Bayroyt Universitetinin tədqiqatçıları ilk dəfə olaraq potensial xərçəng əleyhinə agent olan fostriesinin biosintetik mexanizmindəki əsas addımları deşifrə ediblər. Professor Dr. Frank Hahnın rəhbərlik etdiyi komanda, prosesdə iştirak edən bütün fermentləri laboratoriyada istehsal etməyə və onları nəzarətli şəraitdə fərdi olaraq araşdırmağa müvəffəq olub. Uzunmüddətli perspektivdə tapıntılar birləşmənin daha səmərəli istehsalına yol aça və xərçəng müalicəsində yeni yollar aça bilər. Tədqiqatçılar tapıntılarını Nature Communications jurnalında dərc ediblər .
Xərçəng hüceyrələri nəzarətsiz hüceyrə bölünməsi ilə xarakterizə olunur. Buna görə də bir çox xərçəng dərmanı, məsələn, xərçəng hüceyrələrinin böyüməsi və çoxalması üçün tələb olunan spesifik fermentləri bloklamaqla hüceyrələrin bölünmə qabiliyyətini maneə törətməyi hədəfləyir. Fostriesin, siqnal yollarını pozaraq xərçəng hüceyrələrinin ölümünə səbəb ola bilən bakteriyalar tərəfindən istehsal olunan perspektivli təbii məhsuldur. Lakin, fostriesinin xərçəng əleyhinə vasitə kimi araşdırılmasını nəzərdə tutan əvvəlki klinik sınaqlar dayandırılmalı idi, çünki birləşmə kifayət qədər miqdarda və təmizlikdə əldə edilə bilmədi. Bundan əlavə, fostriesinin qeyri-sabitliyi və müəyyən struktur xüsusiyyətləri onun dərman kimi inkişafını çətinləşdirir.
Buna görə də Bayroytdakı tədqiqat qrupu bu potensial xərçəng əleyhinə agentin əsasını təşkil edən biosintetik mexanizmin mühüm bir hissəsini – uzunmüddətli perspektivdə fostriesinin daha səmərəli və davamlı istehsalına imkan verə biləcək bir irəliləyişi aydınlaşdırmışdır. Bu, təbii məhsulun gələcəkdə yeni və effektiv xərçəng müalicələri üçün əsas ola biləcəyi ehtimalını artırır.
Bayroyt Universitetinin Üzvi Kimya IV tədqiqat qrupunun rəhbəri professor Hanın rəhbərlik etdiyi komandanın tədqiqatının mərkəzində sözdə farmakofor, yəni molekulun əsasən onun farmakoloji aktivliyindən məsul olan struktur komponentləri və xüsusiyyətləri dayanırdı. Hahn deyir: “Tədqiqatımızda ilk dəfə olaraq laboratoriyada fostriesin farmakoforunun qurulması üçün vacib olan bir neçə fermenti istehsal etməyə və onları hüceyrə xaricində nəzarətli şəraitdə fərdi olaraq öyrənməyə nail olduq”.
Tədqiqatçılar həmçinin ilk dəfə olaraq bütün bu fermentlərin tək bir qabda birləşdirildikdə farmakofor əmələ gətirmək üçün birlikdə işlədiyini göstəriblər. “Bu, müasir sintez texnologiyalarının inkişafı üçün olduqca həyəcanvericidir, çünki həm iqtisadi, həm də ekoloji səbəblərə görə mümkün qədər az səylə mürəkkəb molekulların istehsalına artan maraq var. Enzimatik sintez burada böyük potensial təklif edir”, – deyə Hahn izah edir.
Tədqiqatın digər diqqətəlayiq tapıntısı əvvəllər məlum olmayan fermentativ aktivliklərin kəşfi idi: Farmakofor əmələ gəlməsi zamanı tioesteraza iki vacib mərhələni yerinə yetirir – malon turşusunu ötürür və halqa quruluşu əmələ gətirir. İndiyə qədər tək bir fermentin hər iki funksiyanı yerinə yetirə biləcəyi məlum deyildi. Daha sonra yeni bir demalonilaza malon turşusunu parçalayır və xərçəng hüceyrəsindəki hədəf zülalla qarşılıqlı təsir göstərən farmakoforun hissəsini əmələ gətirir. Farmakoforun əmələ gəlməsi üçün vacib olan tioesteraza, demalonilaza və farmakofora xarakterik bir fosfat esteri daxil edən kinaz arasındakı incə tənzimlənmiş qarşılıqlı təsirdir.
“Bu, bioaktiv son məhsulun əmələ gəlməsini optimallaşdırır. Bu üç fermentin dəqiq koordinasiyası olmadan, bakteriyadakı fostriesin biosintez yolu sızan bağ şlanqına bənzəyərdi: bakteriya fostriesin istehsalına xeyli vəsait sərf etsə də, proses çox vaxt istənilən bioaktiv molekulu vermir, çünki qeyri-aktiv və qeyri-sabit aralıq maddələr əmələ gəlir və parçalanır”, – deyə Hahn izah edir.
Əlavə tədqiqatlarda komanda strukturla əlaqəli təbii məhsulların biosintezinə dair fikirlərini genişləndirməyi və müəyyən edilmiş biosintetik fermentləri hədəflənmiş kemoenzimatik sintezdə istifadə etməyi hədəfləyir. Bu yanaşma sintetik kimyanın güclü tərəflərini biotexnologiyanın güclü tərəfləri ilə birləşdirir və onu xüsusilə güclü edir.