Struktur əsaslı RNT neyro-əzələ xəstəliklərinin müalicəsinə səbəb ola bilər
Amy Pavlak Laird, Carnegie Mellon Universiteti tərəfindən
redaktə edən: Gaby Clark , rəy verən: Andrew Zinin
Tercih edilən mənbə kimi əlavə edin
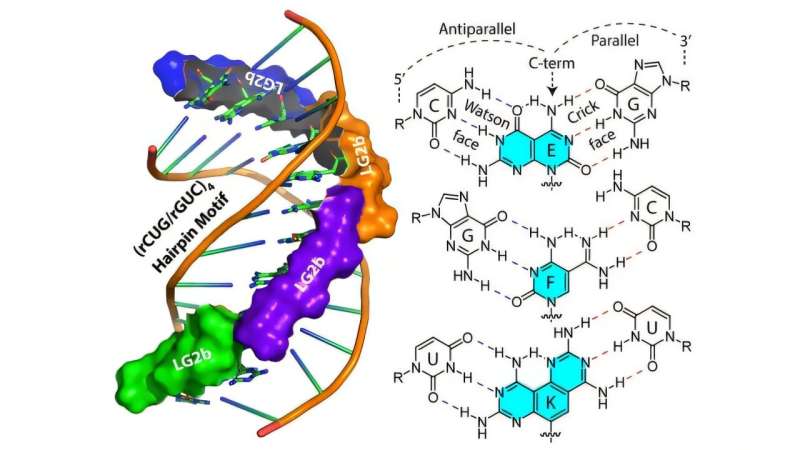
Ligandın spiralların içərisində (solda) və spiralın molekulyar konturu olan ikiqat spiralın kompüter tərəfindən yaradılan təsviri. Mənbə: Karnegi Mellon Universiteti
Karnegi Mellon Universitetinin tədqiqatçıları, yetkinlərdə ən çox rast gəlinən əzələ distrofiyası forması olan 1-ci tip miotonik distrofiya (DM1) və digər RNT təkrar genişlənmə xəstəlikləri üçün yeni müalicə variantlarına səbəb ola biləcək RNT-ni hədəf almağın bir yolunu kəşf etdilər.
Mellon Elm Kollecinin kimya professoru və Biomolekulyar Dizayn və Kəşf İnstitutunun direktoru Danith Ly bildirib ki, “Bu kəşf daha az yan təsirləri və daha geniş tətbiqləri olan yüksək selektiv, struktur əsaslı RNT terapiyalarının inkişafı üçün yol açır. Dəqiq hədəfləmə imkanları ilə bu yanaşma, bu zəiflədici genetik xəstəliklərdən əziyyət çəkən xəstələr üçün effektiv, xəstəliyi dəyişdirən terapiyaların hazırlanması istiqamətində ümidverici bir addımdır.”
Tədqiqat ” Proceedings of the National Academy of Sciences” jurnalında dərc olunub .
Əzələ distrofiyasına səbəb olan nədir?
DM1 kimi vəziyyətlər müəyyən RNT ardıcıllıqlarının çox dəfə təkrarlanması və normal hüceyrə funksiyasına mane olan zərərli strukturlar əmələ gətirməsi zamanı baş verir. Tədqiqatçıların yeni yanaşması, spinocerebellar ataksiya , Fridreyx ataksiyası və amiotrofik lateral skleroz (ALS) kimi xəstəliklər üçün daha az yan təsirləri olan RNT terapiyalarının inkişafına yol açaraq, dəqiq RNT hədəflənməsi üçün güclü və çox yönlü bir həll yolu təqdim edir.
Dünyada hər 2300 nəfərdən ən azı 1-də rast gəlinən DM1 əsasən əzələ itkisinə, zəifliyə və miotoniyaya səbəb olur, lakin ürək, ağciyərlər və gözlər də daxil olmaqla bədənin digər hissələrinə də təsir göstərə bilər. Hal-hazırda effektiv müalicə yoxdur.
DM1, DMPK genindəki mutasiyadan qaynaqlanır və bu da CTG təkrarları kimi tanınan genetik kodun təkrarlanan hissəsində anormal artıma səbəb olur. Bu genetik “kəkələmə” bədənin təlimatları təkrarlananda ilişib qaldıqda baş verir. DM1 olmayan insanlarda bu CTG ardıcıllığı beş ilə 35 dəfə arasında təkrarlanır. DM1 olan bir insanda təkrarların sayı minlərlə ola bilər.Danith Ly, bu kəşfin daha az yan təsirləri və daha geniş tətbiqləri olan yüksək selektiv, struktur əsaslı RNT terapiyalarının inkişafı üçün yol açdığını söylədi. Mənbə: Carnegie Mellon Universiteti
Gen RNT-yə transkripsiya edildikdə, təkrarlar zənciri saç sancağı halqası əmələ gətirir – vacib zülallar üçün yapışqan tələ kimi fəaliyyət göstərən dolaşıq bir quruluş. RNT birləşməsində mühüm rol oynayan bu zülallar halqanın içərisində ilişib qalır və ya tutulur. Tutulan zülallar öz işlərini görə bilmir və hüceyrələrdə bir çox digər zülalların istehsalına mane olan hüceyrə tıxacını yaradır. Nəticədə, bu pozğunluq DM1 simptomlarına səbəb olur və daha çox təkrar sayı adətən daha ağır simptomlara və daha erkən başlanğıca səbəb olur.
“Miotonik distrofiya, Huntington xəstəliyi və kövrək X sindromu kimi mürəkkəb, həyatı oğurlayan simptomlara malik xəstəliklər, çox sadə görünən yalnız üç nukleobazanın təkrarlanmasından qaynaqlanır”, – deyə Ly bildirib. “Əgər zülalların bu saç düzümündə toplanmasının qarşısını ala bilsək, inanırıq ki, bu xəstəliklərin simptomlarını yaxşılaşdırmağa kömək edə bilərik.”
Zəhərli RNT üçün molekulyar “çuxur doldurucu”
Li komandasının son kəşfini yolun qalan hissəsini narahat etmədən zədələnmiş yerlərə səliqəli şəkildə uyğunlaşan “çuxur doldurucu” ilə müqayisə edir. Bu halda, zərər zəhərli CTG RNT təkrarları nəticəsində yaranır.
Yeni tədqiqatda Ly və onun keçmiş postdoktorluq əməkdaşı Şivaji Thadke, doktorluq dərəcəsi alan Dinithi Perera və üçüncü kurs doktorluq tələbəsi Savani Thrikawala da daxil olmaqla komandası, sağlam RNT-ni pozmadan bu xəstəlik yaradan RNT uzantılarını dəqiq tanıyan və onlara bağlanan nuklein turşusu ligandları adlanan kiçik, yüksək spesifik molekullar yaratdılar. Bu yanaşma hazırda inkişaf etdirilən ənənəvi kiçik molekullu dərmanlar və antisens terapiyalarından daha dəqiqdir və yan təsirlərə səbəb olma ehtimalı daha azdır.
Ly-yə görə, bu cür ənənəvi terapevtik yanaşmalar tez-tez spesifikliklə mübarizə aparır, ya normal və patogen RNT-ni ayırd edə bilmir, ya da effektiv çatdırılma üçün mürəkkəb modifikasiyalar tələb edir. Yeni nuklein turşusu ligandları bu çətinlikləri ikiüzlü tanıma mexanizmi vasitəsilə aradan qaldırır ki, bu da patogen təkrarların dəqiq hədəflənməsini təmin edir və hədəfdən kənar qarşılıqlı təsirləri minimuma endirir.
İki tərəfli molekulyar strategiya
Ly-nin yeni RNT hədəfləmə yanaşmasının dizaynının mərkəzində qamma peptid nuklein turşuları və ikiüzlü (Janus) əsaslar dayanır.
Karnegi Mellonun Nuklein Turşuları Elmi və Texnologiyası Mərkəzindəki Ly və həmkarları, RNT və DNT ilə eyni nukleobazları ehtiva edən sintetik molekullar olan peptid nuklein turşularının (PNA) yaradılmasında və inkişaf etdirilməsində liderdirlər. PNA-lar xəstəliyə səbəb olan genetik ardıcıllıqlara uyğun olaraq proqramlaşdırıla bilər ki, bu da onların zərərli ardıcıllıqları tapıb onlarla əlaqə qurmasına imkan verir. 2014-cü ildə CNAST növbəti nəsil PNA texnologiyasını inkişaf etdirməyə başladı. Ly diqqətini Yanus əsaslı PNA-ların hazırlanmasına yönəltdi. İkiüzlü Roma tanrısı Yanusun adını daşıyan PNA-lar ikitərəflidir və bu da onlara DNT və ya RNT molekulunun hər iki zəncirinə bağlanmağa imkan verir.
“Bu ligandlar, RNT-nin ikinci və üçüncü dərəcəli strukturlarının açılmasını tələb edən ənənəvi antisens yanaşmasından fərqli olaraq, özlərini iki RNT zəncirinin arasına yerləşdirirlər”, – deyə Ly bildirib.
Laboratoriya modellərində aparıcı ligand olan LG2b, normal gen funksiyasına müdaxilə etmədən zərərli protein-RNT komplekslərini sıxışdıraraq xəstəliyə səbəb olan RNT ardıcıllıqları üçün diqqətəlayiq selektivlik nümayiş etdirdi.
Tədqiqat qrupu, ligandları ilə işləməyə davam edir, hüceyrə udulmasını artırmaq üçün onları optimallaşdırır, dərman çatdırılma metodlarını təkmilləşdirir və klinikayaqədərki xəstəlik modellərində effektivliyini qiymətləndirir.
Ly, Thrikawala, Thadke, Perera və CMU məzunu İşa Dhami, eləcə də Hindistan Elm İnstitutunun, Corciya Dövlət Universitetinin və Sinqapurun Nanyang Texnologiya Universitetinin tədqiqatçıları ilə birlikdə nəşr etdirib.
Nəşr detalları
J. Dinithi R. Perera və digərləri, 1-ci tip miotonik distrofiya ilə əlaqəli rCUG təkrarlarının selektiv hədəflənməsi üçün çuxur doldurma strategiyası, Milli Elmlər Akademiyasının materialları (2026). DOI: 10.1073/pnas.2507065123
Jurnal məlumatları: Milli Elmlər Akademiyasının materialları
Klinik kateqoriyalar
NevrologiyaKlinik genetikaKarnegi Mellon Universiteti tərəfindən təmin edilir