Tədqiqatçılar davamlı xərçənglər üçün yeni antikor-RNT terapiyası hazırlayırlar
Yale Universiteti tərəfindən
Sadie Harley tərəfindən redaktə edilmişdir , Andrew Zinin tərəfindən nəzərdən keçirilmişdir
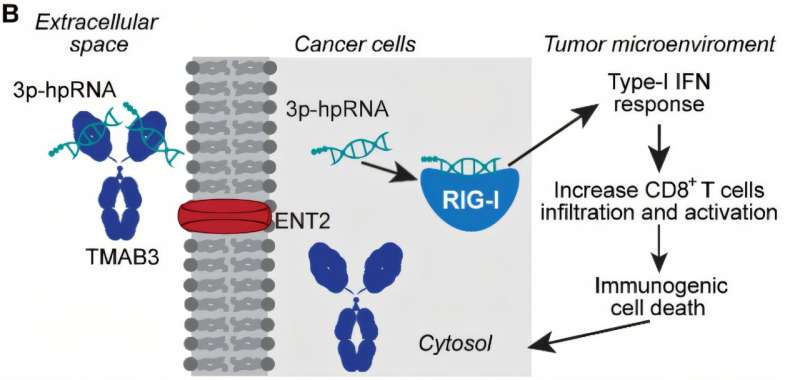
Redaktorların qeydləri3p-hpRNA-nın ENT2 vasitəsilə hüceyrələrə TMAB3 vasitəçiliyi ilə çatdırılmasını təsvir edən, RIG-I tərəfindən tanınmağa və I tip IFN siqnalının aktivləşdirilməsinə səbəb olan sxematik təsvir. Kredit: Elm Tərcümə Tibb (2025). DOI: 10.1126/scitranslmed.adk1868
Elm Tərcümə Tibbində bildirilən bir araşdırmaya görə, RNT müalicəsini çətin əldə edilən və müalicəsi çətin olan şişlərə dəqiq şəkildə çatdıra bilən xüsusi olaraq hazırlanmış antikor, heyvan modellərində sağ qalmağı əhəmiyyətli dərəcədə yaxşılaşdırdı və şiş ölçülərini azaldıb .
Tədqiqat sübut edir ki, qan dövranına yeridildikdən sonra TMAB3 antikoru anadangəlmə immun reaksiyanı stimullaşdıran bir növ RNT ilə birləşərək, şişlərə lokallaşdırıla və mədəaltı vəzi, beyin və dəri xərçənglərində inadkar xəstə hüceyrələrə nüfuz edib məhv edə bilir .
“Şişlərə RNT əsaslı müalicələrin çatdırılması çətin idi. TMAB3-ün RNT yüklərini şişlərə çatdıra bilən antikor/RNT kompleksləri yarada bilməsi bizim tapdığımız bu problemin öhdəsindən gəlmək üçün yeni bir yanaşma təmin edir” Peter Glazer, baş müəllif və Robert E. Hunter, YaSMedicinele Tibb Məktəbinin Terapevtik Radiologiya və Genetika üzrə professoru deyir.
Glazer və Yale ilk müəlliflərindən əlavə Elias Quijano, Ph.D.; Diana Martinez-Saucedo, Ph.D.; Zaira İanniello, fəlsəfə doktoru; və Nataşa Pinto-Medici, Ph.D., Yale’nin Terapevtik Radiologiya Departamentindən və genetika, molekulyar biofizika və biokimya, biotibbi mühəndislik , patologiya və tibbi onkologiya departamentlərindən və üçü İllinoys Urbana-Champa Universitetindən olan 25 digər töhfəçi var.
Xüsusilə, adətən standart müalicələrə və ən yaxşı immunoterapiyaya davamlı olan üç növ “soyuq” şişin heyvan modelləri – mədəaltı vəzi xərçəngi , medulloblastoma (beyin xərçənginin bir növü) və melanoma (dəri xərçəngi) – xərçəng hüceyrələrinə yerləşdirilən, əsasən sağlam toxumalardan qaçan dəqiq müalicəyə əhəmiyyətli cavab verdi.
Nəticələr:
- Pankreas kanalının adenokarsinoması üçün heyvan modelində müalicə xərçəng hüceyrələrinə hücum edən CD8 + T hüceyrələrinin varlığını artırmaqla şişlərin ölçüsünü əhəmiyyətli dərəcədə azaldıb və sağ qalma müddətini uzadıb .
- Medulloblastoma heyvan modelləri eyni şəkildə cavab verdi. Müalicə qan-beyin baryerini keçərək şişlərə çatmaq və kiçilmək və sağlam toxumanın girov müalicəsi nəticəsində yarana biləcək bir immun reaksiyaya səbəb olmadan sağ qalma müddətini uzatdı.
- Melanoma olan heyvan modellərində şişin açıq şəkildə basdırılmış böyüməsi və ciddi yan təsirlərin və ya toksikliyin olmaması qeyd edildi.
Tədqiqatçılar antikoru dəyişdirmək üçün kompüter modelləşdirməsindən istifadə edərək, onu RNT-yə bağlamağa imkan verdilər və həmçinin onu “insaniləşdirdilər” ki, orqanizm ona bir işğalçı kimi hücum etməsin, mümkün klinik istifadəyə doğru bir addım.
“Bu iş RNT əsaslı terapiyaların klinikaya çevrilməsi üçün təməl qoyur. Sistemli toksiklik olmadan şiş hüceyrələrinə məqsədyönlü çatdırılmaya nail olmaqla, biz təkcə şişə xas deyil, həm də hər bir xəstənin xərçənginin immunoloji kontekstinə uyğunlaşa bilən müalicələrin inkişaf etdirilməsi imkanını açırıq” dedi. terapevtik radiologiya və molekulyar biofizika və biokimya.
“Daha inkişaf etməklə, bu platforma fərdiləşdirilmiş immuno-RNT terapiyalarını dəstəkləyə və insanda ilk klinik sınaqlara doğru irəliləyə bilər.”
Ətraflı məlumat: Elias Quijano və digərləri, RNT bağlayan və hüceyrəyə nüfuz edən antikorun sistemli tətbiqi, terapevtik RNT-ni xərçəngin çoxsaylı siçan modellərinə hədəfləyir, Elm Tərcümə Tibb (2025). DOI: 10.1126/scitranslmed.adk1868
Jurnal məlumatı: Science Translational Medicine Yale Universiteti tərəfindən təmin edilmişdir